
Axel Abelein, docent vid Karolinska institutet
Den nya bromsmedicinen Leqembi är ett stort framsteg för alzheimerforskningen, men det behövs nya infallsvinklar för att komma framåt. Axel Abelein, gruppledare och docent vid Karolinska Institutet, hoppas att anti-amyloidproteinet BRICHOS kan vara en möjlig framtida behandlingskandidat.
Det var tidigare observationer att ett protein som kallas BRICHOS påverkar aggregering av andra aggregeringsbenägna proteiner som gav forskarna idén. Kan BRICHOS vara en spelare som kan påverka aggregeringen av de giftiga proteinformerna i hjärnan vid Alzheimers sjukdom?
"Vår approach är att titta på det som finns naturligt i kroppen. BRICHOS är en så kallad chaperon eller ett stödjeprotein som bland annat ser till att proteinerna veckar sig rätt och inte klumpar ihop sig. Vi försöker förstå hur BRICHOS beter sig och om det i framtiden kan användas som något slags behandling", berättar Axel Abelein när vi ses på NEO - ett nav för grundläggande och klinisk forskning i Flemingsberg, som är en del av Karolinska Institutet.
Hos en person med svår Alzheimers finns det amyloida plack i hjärnan. Det är proteinet beta-amyloid som klumpar ihop sig i allt större aggregat, från monomerer till oligomerer, fibriller och slutligen till plack. En av forskarnas hypoteser är att det är oligomererna som är mest giftiga och förstör nervcellerna.
"I våra försök har vi sett hur aggregeringen av beta-amyloid går långsammare när vi tillsätter BRICHOS. Chaperonproteinet binder till fibrillytan och hindrar oligomerbildningen och den har liknande effekt på tau och även på alfasynuklein, det protein som anses ligga bakom Parkinsons sjukdom", berättar Axel Abelein.
Axel och hans forskarteam studerar hur BRICHOS påverkar klumpbildningen av beta-amyloid i provrör rent biokemiskt, medan hans kollegor på NEO, under ledning av professor Jan Johansson, bland annat har gjort försök med musmodeller. I de försök som gjorts på möss har chaperonet visat sig mildra den neuroinflammation som de amyloida placken ger upphov till men även påverka mössens beteende så att de mår och fungerar bättre.
"De försök vi har gjort ser mycket lovande ut. Vi hoppas att det vi ser i vårt labb i slutändan även ska kunna appliceras på människor. Det fina med BRICHOS är att det är en del av kroppens eget försvarssystem, men även att det tar sig över blod-hjärnbarriären i mycket större mängder jämfört med antikroppar."
Sammanfattningsvis hoppas Axel Abelein att BRICHOS ska kunna underlätta förståelsen av de molekylära mekanismerna bakom amyloidbildning och bidra till effektiva behandlingsmetoder mot Alzheimers sjukdom och Parkinsons sjukdom.
Vad driver dig att forska kring Alzheimers sjukdom?
"Jag vill nog säga att min huvudsakliga drivkraft är att jag vill arbeta med att hjälpa människor, de neurodegenerativa sjukdomarna drabbar så många. Det känns viktigt och spännande att kunna bidra."
Vad betyder anslaget på 850 000 kronor från Alzheimerfonden för dig?
"Det är mycket värdefullt. Det gör det möjligt att finansiera en stor del av en postdoktor-tjänst och genomföra vårt forskningsprojekt."

Henrik Ahlenius, universitetslektor vid Lunds universitet
Henrik Ahlenius, universitetslektor och forskargruppschef Stamcellscentrum vid Lunds universitet har fått ett anslag på 1,3 miljoner av Alzheimerfonden. Med hjälp av stamcellsbaserade modeller hoppas han komma närmare förståelsen av gliacellernas roll i utvecklingen av Alzheimers sjukdom.
Stamcellsforskningen har tagit enorma kliv de senaste tio-femton åren. Sedan länge kan forskarna till exempel använda mänskliga hudceller för att skapa så kallade inducerat pluripotenta stamceller som kan mogna ut till nervceller. Dessa celler kan i sin tur med hjälp av Crispr (gensaxteknik) modifieras för att efterlikna de nervceller som finns i en mänsklig hjärna som drabbats av Alzheimers sjukdom och på så sätt användas i forskningen kring neurodegenerativa sjukdomar.
Nyligen identifierade forskarna astrocyterna, en av hjärnas stödjeceller eller gliaceller, som en nyckelspelare i utvecklingen av Alzheimers sjukdom. Tidigare har forskarna varit hänvisade att använda möss för att få fram primära astrocyter till sin forskning. Men 2018 kom Henrik Ahlenius och hans forskargrupp med spännande resultat – en ny metod för att snabbt och effektivt generera mänskliga astrocyter från pluripotenta stamceller.
I det forskningsprojekt som Henrik Ahlenius nu har fått ett anslag för ligger fokus på att utforska just gliacellernas roll i utvecklingen av Alzheimers sjukdom:
"Man kan säga att vi har inspirerats av musmodellerna och med hjälp av inducerat pluripotenta stamceller skapat artificiella modeller av nervceller hos riktigt sjuka patienter. Vi hoppas att dessa artificiella Alzheimers celler gör att vi effektivt kan studera sjukdomsmekanismerna"säger Henrik Ahlenius och fortsätter:
"Om vi kombinerar de olika stamscellsmodellerna för nervceller och gliaceller kan vi studera hur de olika hjärncellerna interagerar och vilken roll gliaceller har i utvecklingen av sjukdomen. Reagerar gliacellerna dysfunktionellt? Hjälper de nervcellerna eller förvärrar de läget i en negativ loop?"
Henrik Ahlenius och hans forskargrupps hypotes är att gliacellerna bidrar till utvecklingen av symptomen vid Alzheimers sjukdom men även att de i framtiden kommer att kunna användas som biomarkörer för tidig upptäckt av sjukdomen och bidra till utvecklingen av nya läkemedel.
I forskningsprojektet kommer de nya stamcellsbaserade modellerna kombineras med avancerad proteomik och transkriptomik (metod för att studera genuttryck), för att studera gliacellernas roll i utvecklingen av sjukdomen. Det forskarna hittar under projektets gång kommer att valideras genom studier av och prover från patienter i form av ryggvätske- och blodprov samt vävnadsprov från avlidna patienter.
"Det behövs nya angreppssätt för diagnostisk och terapi. Jag är övertygad om att vi kommer få fram ny intressant kunskap från de här modellerna och hitta nya biomarkörer och nya mål för framtida terapier", säger Henrik Ahlenius.
Vad betyder anslaget på 1,3 miljoner från Alzheimerfonden för dig?
"Det känns jätteroligt. Det är en kostsam forskning vi bedriver. Anslaget gör att vi kan driva den mer effektivt och att en av våra postdoktorer kan fortsätta sitt arbete. Pengarna kom mycket bra i tiden."

Nicholas Ashton, Assistant Professor vid Göteborgs universitet
Nicholas Ashtons intresse för demensforskning väcktes när han studerade klinisk neurovetenskap på masternivå vid King's College London. Sedan 2018 är han verksam som forskare vid Göteborgs universitet. Under 2022 har han tilldelats 1,2 miljoner kronor av Alzheimerfonden till sin forskning och ett stipendium på 1 miljon kronor till en doktorandtjänst för vilken han kommer att fungera som handledare.
Grattis till anslaget från Alzheimerfonden! Hur känns det?
"Som forskare känns det självklart mycket bra att få stöd till sin forskning. Det är extra viktigt att Alzheimerfonden satsar på yngre forskare så att vi får möjlighet att testa nya fräscha idéer på de utmaningar som Alzheimerforskningen står inför de kommande två decennierna. Det vi åstadkommer nu kommer att påverka utvecklingen inom området i tio-tjugo år framåt."
Nicholas Ashton ingår i en forskargrupp inom neurokemi vid Göteborgs universitet som varit mycket framgångsrik med att ta fram blodbiomarkörer som kan kopplas till sjukdomsutvecklingen av Alzheimers sjukdom. Biomarkören p-tau217 har visat sig kunna spåra förändringar i sjukdomen i ett mycket tidigt skede av sjukdomsprocessen. Att kunna använda enkla blodprov i stället för kostsamma undersökningar med avancerad bilddiagnostik och inte helt smärtfria prover i ryggvätska öppnar nya vägar inom alzheimerforskningen och jakten på nya läkemedel.
Nicholas Ashton berättar att de 1,2 miljoner som han nu tilldelats av Alzheimerfonden kommer att användas för att ta nästa stora steg – att utveckla ett blodtest som öppnar upp för att öka tillgängligheten till tillförlitlig diagnostik. Han beskriver det som ett ”bloodspot test” – enkelt att ta själv hemma. Man får hemskickat ett test-kit via en vårdcentral eller liknande instans och gör ett stick i fingret (precis som personer med diabetes gör vid blodsockermätningar), droppar sedan lite blod på ett kort och skickar det sedan per post till ett laboratorium.
"Känner man sig orolig ska man kunna ta testet via sin ordinarie vårdgivare och skicka in det. Efter analys tänker vi oss att man kommer att få ett samtal där en person med kunskap om hur testet ska tolkas förmedlar resultatet – ser allt bra ut kan man återkomma om ett år till exempel."
"Målet är enkelhet och att blodtesterna i framtiden ska kunna användas även vid andra sjukdomar som ALS och MS, där personer som står på medicinering med hjälp av blodtestet enkelt ska kunna kontrolleras och deras sjukdomsutveckling följas månads- eller veckovis."
Till att börja med kommer hundra patienter vid en Minnesklinik i Göteborg att ingå i studien som senare kommer att utvidgas till övriga Europa. Ett laboratorium i Spanien där det bland annat pågår en studie med personer som har Down syndrom kommer att inkluderas liksom ett forskningsprojekt i England där man kommer att följa upp blodtesterna med kognitiva tester via dator i hemmet.
"Det känns mycket spännande – att testa om det enkla blodprovet fungerar i verkligheten, säger Nicholas Ashton och berättar att för honom handlar forskningsprojektet mycket om inkludering. Människor som bor långt ut i områden med låg tillgänglighet, där det inte finns tillgång till laboratorier och frysar och där demenssjukdomar också är vanliga, ska inte lämnas utanför. Även dessa människor ska kunna testa sig.
Kommer det att fungera? Vi måste i alla fall våga testa. Jag är mycket öppen för de resultat vi kommer fram till, det är inte helt säkert att det är den bästa metoden – men det kan mycket väl vara det."
Under Alzheimerdagen i september fick du ta emot en donation på en miljon kronor till en doktorandtjänst. Hur ska de användas?
"Pengarna kommer att gå till att anställa en doktorand som primärt kommer att undersöka möjligheterna att utveckla ett brett spektrum av proteinanalyser. Idag har vi identifierat de bästa blodbiomarkörerna för att upptäcka tidig Alzheimers sjukdom. Vi behöver hitta liknande biomarkörer för att kunna upptäcka andra demenssjukdomar som till exempel Frontallobsdemens. Detta kommer doktoranden att arbeta med."
Vad hoppas du uppnå med din forskning?
"Mitt mål är att det i framtiden ska finnas ett enkelt och lättillgängligt blodtest som gör att vi kan upptäcka demenssjukdomar på ett tidigt stadium, långt innan symptomen dyker upp. Ett blodtest som kan övervaka sjukdomsutvecklingen och ge patienterna befintlig behandling så fort som möjligt."
Nicholas Ashton, tilldelades ”Drottning Silvias pris till en ung alzheimerforskare”. I september 2021 fick han ta emot det prestigefulla priset på 125 000 kronor.

Kaj Blennow, professor Göteborgs universitet
Kaj Blennows arbete med blodbaserade biomarkörer har revolutionerat diagnostiken av Alzheimers sjukdom. 2023 tilldelades den prisade professorn och överläkaren vid Sahlgrenska Universitetssjukhuset tilldelades 1,5 miljoner av Alzheimerfonden för att utveckla ännu mer träffsäkra biomarkörer.
Kaj Blennow har haft enorm betydelse för Alzheimer-forskningen. Hans första viktiga genombrott var den banbrytande analysen av biomarkörerna beta-amyloid och P-tau i cerebrospinalvätska. Därefter utvecklade han nya analysmetoder med den ultrakänsliga Simoa (Single molecule array)-tekniken som gör det möjligt bestämma koncentrationen av olika varianter av P-tau i vanliga blodprover, vilket kan predicera vilka patienter som kommer att utveckla Alzheimers sjukdom.
Nu är siktet inställt på att utveckla två nya varianter av tau-analyser.
Varför och vad är syftet?
"De blodtester som finns idag fungerar bra för att identifiera Alzheimers sjukdom, vi kan mäta 3–4 varianter av P-tau som är tätt sammankopplade med utvecklingen av sjukdomen. Men en associationskoppling är inte samma sak som orsakssammanhang", förklarar Kaj Blennow.
Han och hans team har studerat något de kallar MTBR-tau-fragment och ser ett tydligare samband med utvecklingen av sjukdomen. MTBR-tau-fragment är den biten av tau som aggregerar – alltså via en biokemisk process klumpar ihop sig till så kallade tangles, som hindrar transporten av viktiga ämnen i nervcellerna.
"Genom att mäta MTBR-tau-fragment i plasma får vi en mer direktkopplad och mer lättolkad markör, ett mer direkt mått kopplat till sjukdomsutvecklingen", säger Kaj Blennow.
Målet för Kaj Blennow och hans team är nu att utveckla ultrakänsliga Simoa-analyser som gör det möjligt att mäta tau368 och andra MTBR-tau-fragment. De kommer också använda avancerade metoder inom exempelvis masspektrometri för att verifiera MTBR-tau-peptider i plasmaprover.
Vad hoppas du åstadkomma med din forskning?
"Om vi lyckas kommer vi att ha nya biomarkörer som är mer kopplade till sjukdomen. Jag hoppas att vår forskning leder till att vi kan förstå sjukdomen bättre, förstå hur tidigt tau-patologin i Alzheimer uppkommer och hur den är kopplad till olika symptom. Min förhoppning är också att kunna studera de nya biomarkörerna i kliniska forskningsstudier och på sikt bidra till utvecklingen av nya läkemedel."
Vad kommer forskningsanslaget användas till?
"Det kommer att gå mycket till lab-kostnader, till instrument, reagens och liknande men även till personalkostnader."

Tomas Deierborg, professor vid Lunds universitet
Tomas Deierborg, professor och forskningschef på laboratoriet för Experimentell Neuroinflammation vid Lunds universitet, har fått ett anslag på 1,3 miljoner kronor. I sitt forskningsprojekt undersöker han den roll det inflammatoriska proteinet galectin-3 har i utvecklingen av Alzheimers sjukdom och möjligheterna att vidareutveckla en gal3-hämmare.
Tomas Deierborg och hans forskargrupp i Lund var först med att påvisa att proteinet galectin-3, som framför allt ansamlas i hjärnans mikrogliaceller, spelar en nyckelroll i utvecklingen av Alzheimers sjukdom.
"Galectin-3 har en viktig roll i många av de skeenden som är inblandade i den kroniska inflammation som uppstår vid Alzheimers sjukdom. Vi har gjort många olika studier och ser hela tiden att proteinet korrelerar väl med sjukdomen och påverkar sjukdomsprocesserna negativt", säger Tomas Deierborg.
När han och hans teams nya forskningsrön om galectin-3 publicerades ansågs de så intressanta att ett amerikanskt företag påbörjade utvecklingen av en ”hämmare” eller en antikropp som kan binda det inflammatoriska proteinet så att det inte blir skadligt. Antikroppen har även testats i kliniska studier.
I Tomas Deierborgs nya forskningsprojekt är en av ingångarna att testa nya hämmare som utvecklas i samarbete med kemiprofessor Ulf Nilsson i Lund och som kan testas i Tomas experimentella modeller för Alzheimers sjukdom.
"Kan vi hitta en ny hämmare som kan binda in till galectin-3 och optimera den så att den kan ta sig in i hjärnan över blod-hjärnbarriären? Vad fungerar bäst, att injicera drogen rätt in i hjärnan, ta det nasalt eller centralt i blodet? Det är några av de frågeställningar vi arbetar med", berättar Tomas Deierborg.
I en annan del av projektet studerar man vad som kan påverka utvecklingen av Alzheimers sjukdom. Ett spår är att i musmodeller undersöka om det är möjligt att träna upp djurens immunförsvar. Mössen injiceras med Lipopolysackarider (LPS), ett inflammatoriskt ämne som bildas av bakterier, som aktiverar immunförsvaret och som senare kan påverka sjukdomsutvecklingen.
"Man kan säga att vi tränar immunförsvaret för att se om det kan bli bättre på att i ett senare skede kunna motverka Alzheimers sjukdom."
Ännu ett spår är att undersöka vilken roll riskgenen AOPE4 har i utvecklingen av Alzheimers sjukdom. Cirka en tredjedel av svenskarna har denna riskgen som ökar risken att drabbas av Alzheimers sjukdom 3-12 gånger beroende på om man har en kopia från en förälder eller två kopior från båda sina föräldrar.
"Vi tittar på olika saker som kan påverka sjukdomen, jobbar med olika angreppsvinklar för att kunna förstå hur hjärnans inflammatoriska mikrogliaceller påverkar sjukdomen. Vi hoppas hitta centrala mekanismer för sjukdomsutvecklingen, för att sedan kunna hitta rätt substanser/hämmare som förhoppningsvis kan gå vidare för att testas på patienter."
"En stor fördel här i Lund är att vi dels har tillgång till forskningsanläggning Max IV där vi kan studera molekyler på atomnivå, men även vårt nära samarbete med forskare som Ulf Nilsson på Kemicentrum och Hakon Leffler som har stor erfarenhet av de mekanismer vi studerar."
Tomas Deierborg är helt övertygad om att han och hans forskarteam har valt rätt inriktning – att galectin-3 spelar en avgörande roll i utvecklingen av Alzheimers sjukdom.
"Ja, vi har många spår ute nu och satsar hårt på det här. Vi ska göra vad vi kan för att göra skillnad och bidra med att nå ut till patienterna med ett nytt läkemedel."
Vad betyder forskningsanslaget på 1,3 miljoner från Alzheimerfonden?
"Jag är oerhört glad för anslaget. Utan Alzheimerfonden hade det inte blivit någon forskning, utan fondens hårda arbete hade det inte fungerat. Det var tack vare mitt första anslag, som jag fick 2014 av Alzheimerfonden, som jag kunde starta upp denna forskningslinje."

Anna Erlandsson
Anna Erlandsson, professor vid Uppsala universitet
Anna Erlandsson, professor vid Institutionen för folkhälso- och vårdvetenskap Uppsala universitet, tilldelades 1,3 miljoner kronor - ett av de största anslagen 2024. Hon och hennes team studerar zombosomers roll för spridningen av Alzheimers sjukdom i hjärnan.
Alzheimerforskningen har under många år varit inriktad på förändringar som sker i nervcellerna under sjukdomsförloppet. Men under de senaste åren har intresset för hjärnans stödjeceller exploderat. Den vanligaste typen av stödjecell är astrocyten som har visat sig vara en viktig spelare i utvecklingen av Alzheimers sjukdom.
Anna Erlandsson och hennes forskarteam har tidigare visat att astrocyter tar upp stora mängder amyloid-beta och tau, men är mycket långsamma när det gäller att bryta ner det intagna materialet. Forskargruppens resultat tyder på att astrocyterna har en central roll i den kroniska inflammation som uppstår vid sjukdomen och bidrar till att sprida den i hjärnan.
Nu är forskarteamet först med att upptäcka en helt ny form av astrocytiska strukturer som fått namnet zombosomer.
"Vi har filmat cellkulturer av mänskliga hjärnceller och noterat att astrocyterna utsöndrar en sorts miniceller, som till skillnad från alla tidigare beskrivna vesiklar rör sig aktivt. Våra resultat indikerar att dessa zombosomer kan ha en otrolig kapacitet att sprida giftiga proteinaggregat från en cell till cell och på så sätt starta sjukliga processer", säger Anna Erlandsson och berättar att zombosomer har fått sitt namn av att de inte har någon cellkärna men ändå rör sig och tycks vara ”levande”.

Bildtext: Två astrocyter och en zombosom. Pilen visar zombosomen.
Syftet med projektet är att utforska zombosomernas roll i spridningen av de giftiga proteinerna och även undersöka om det går att påverka astrocyterna så att sjukdomsförloppet kan bromsas.
"Våra analyser visar att zombosomer innehåller en speciell form av proteinet vimentin. Vi kommer att undersöka det i detalj och ta reda på om vi kan använda specifika vimentininhibitatorer för att hindra att skadliga zombosomer utsöndras från astrocyterna. Här tror jag att vi kan lära oss mycket av de framsteg som gjorts inom tumörbiologin."
"Om vi förstår sjukdomsmekanismerna – hur patologin sprids till nya delar av hjärnan – är jag övertygad om att vi kan få fram effektiva mediciner, avslutar Anna Erlandsson."

Daniel Ferreira
Daniel Ferreira, docent vid Karolinska institutet
Daniel Ferreira, docent i neuropsykologi och föreståndare för Centrum för Alzheimerforskning vid Karolinska institutet, tilldelades 2023 ett anslag på 1,9 miljoner kronor av Alzheimerfonden.
"Jag är så glad att fonden väljer att satsa på Lewykroppssjukdom. Vår forskning är mycket kostsam och det krävs stora anslag för att utveckla den", säger Daniel Ferreira.
Lewykroppssjukdom är den näst vanligaste formen av neurodegenerativa hjärnsjukdomar efter Alzheimers sjukdom. Den uppkommer när proteinet alfa-synuklein felveckas i hjärnan, klumpar ihop sig och bildar så kallade Lewykroppar, vilket skadar nervcellerna.
Att demenssjukdomarna ofta inte är ”rena” sjukdomar utan interagerar med varandra är en kunskap som har slagit igenom i forskarvärlden. En patient som fått diagnosen Levykroppssjukdom kan ofta även ha Alzheimers sjukdom, vaskulär sjukdom, och andra hjärnsjukdomar. Hos patienter med Alzheimers sjukdom kan så många som 30–40 procent ha en blanddiagnos och även lida av Levykroppssjukdom.
"Vi måste öppna våra ögon för att det förhåller sig så. Om vi förstår komplexiteten kan vi fortare få fram en bra behandling och utveckla avancerade läkemedel som riktar sig mot samtliga sjukdomar och kan lindra eller bota dem", säger Daniel Ferreira.
Störd sömn och nedsatt luktsinne är tidiga indikatorer på Lewykroppssjukdom. De senaste åren har stora framsteg gjorts inom diagnostiken. Idag kan ett ryggvätskeprov avslöja om en patient har det felveckade proteinet. Vävnadsprov i näsan och på huden är nya metoder som testas och det finns stora förhoppningar att inom en snar framtid kunna utveckla ett blodprov.
"Jag och min forskargrupp arbetar med att utveckla de diagnostiska verktygen. Vi kombinerar undersökning med PET-kamera, MRI (magnetisk resonans-tomografi), ryggvätskeprov, biomarkörer och tar AI till hjälp för att analysera våra data. Målet är att hitta nya och enklare metoder att identifiera sjukdomen som ska kunna användas kliniskt inom sjukvården."
I projektet kommer forskargruppen bland annat att med hjälp av MRI undersöka hjärnvävnad från avlidna patienter som levt med sjukdomen. Detta sker i ett unikt samarbete med biobanker i Madrid och Amsterdam.
"Med hjälp av bilderna vi får kan vi jämföra hur det ser ut hos friska patienter men också med patienter som har Alzheimers sjukdom. Många patienter har båda sjukdomarna på olika nivåer, de överlappar varandra och är svåra att identifiera. Vi måste försöka förstå komplexiteten i sjukdomarna för att kunna ta fram behandlingar som verkligen kan hjälpa."
Vad betyder anslaget på 1,9 miljoner kronor för dig?
"Det möjliggör att vi kan anställa tre personer på heltid och accelerera vår forskning. Anslaget bidrar också till att vi kan locka de bästa experterna inom området till Sverige. Mayo Clinic i USA är ett av universiteten som gärna vill inleda ett samarbete."

Emma Gerrits
Emma Gerrits, postdoktor vid Karolinska institutet
Emma Gerrits är postdoktor vid Institutionen för neurovetenskap vid Karolinska institutet. 2023 beviljades hon 1,2 miljoner av Alzheimerfonden för att komma närmare förklaringen till hur frontotemporal demenssjukdom utvecklas.
"Mejlet från Alzheimerfonden gjorde mig först chockad sedan väldigt glad", säger den nederländska forskaren, som med sina 29 år är den yngsta någonsin att beviljas ett sådant stort anslag.
Frontotemporal demenssjukdom (FTD), år en av de vanligaste formerna av demenssjukdom hos personer under 65 år. Man beräknar att den till 30 procent är ärftlig och kopplar ett protein som benämns TDP-43 till utvecklingen av sjukdomen.
För två år sedan gjorde ett stort genombrott inom FTD-forskningen. Med hjälp av enkelcells-RNA-sekvensering, en teknik som ger möjlighet att studera biologiska funktioner i varje enskild cell i taget, studerade nederländska forskare hjärnceller från patienter som avlidit i sjukdomen.
"Det var första gången man på det här sätt undersökte hjärnvävnad från människor och inte från möss. Forskarna upptäckte något spännande – att de vaskulära cellerna och astrocyterna var starkt påverkade medan hjärnans immunceller, mikroglian, såg nästan normala ut", berättar Emma Gerrits.
I det projekt som beviljats pengar bygger hon nu vidare på kollegornas forskningsresultat. Med en ny teknik som heter spatial transcriptomik kommer hon att analysera frontala, temporala och occipitala cortexprover från personer som avlidit med FTD och jämföra dem mot köns- och åldersmatchade vävnadsprover.
"Vi har en stor fördel som kan få tag i hjärnvävnad från banken i Nederländerna. I till exempel USA har man mycket striktare reglering kring hantering av vävnad från avlidna personer. Vi har också tillgång till den allra senaste tekniken genom ett samarbete med företaget BGI Research i Kina."
Med en kombination av enkelcells-RNA-sekvensering och spatial transcriptomik är det möjligt för forskarna att studera en cell i taget och få en ögonblicksbild av genaktiviteten i var och en av dem. De kan samtidigt se var cellerna befinner sig i vävnaden och vilken relation de har till varandra.
"Vilka celler finns i vävnadsprovet och hur kommunicerar de? Vilka gener uttrycker vilka proteiner och vad kan de berätta om sjukdomsutvecklingen", förklarar Emma Gerrits sin forskning och berättar att undersökningen av vävnadsproven är den lilla delen av arbetet.
När den är genomförd vidtar det stora arbetet med att gå igenom alla data, vilket kommer att ta flera år av programmering och analys.
Vad hoppas du åstadkomma med din forskning?
"När vi förstår vad som händer i cellerna kan det hjälpa oss att hitta biomarkörer för sjukdomen, som i sin tur som kan hjälpa till vid diagnosticering och att ta fram läkemedel. Det kommer inte att hända nu eller om fem år men förhoppningsvis i framtiden."

Vilmantas Giedratis
Vilmantas Giedraitis, forskare vid Uppsala universitet
Vilmantas Giedraitis, forskare vid institutionen för folkhälso- och vårdvetenskap vid Uppsala universitet, har 2022 tilldelats en miljon kronor av Alzheimerfonden. Pengarna möjliggör det viktiga arbetet med att kartlägga de genmutationer som orsakar Alzheimers sjukdom.
"Det känns mycket bra att få anslaget från Alzheimerfonden. Det gör att vi kan fortsätta med våra mutationsanalyser och sekvenseringar och gör det möjligt att anställa nya medarbetare", säger Vilmantas Giedraitis, forskare vid Uppsala universitet.
Hos en till två procent av alla som drabbas av Alzheimers sjukdom är sjukdomen ärftlig och orsakas av en mutation på en känd sjukdomsgen. Idag känner forskarna runt om i världen till över 200 mutationer i de tre vanligaste sjukdomsorsakande generna. I Sverige har man hittat genförändringar hos flera släkter bland annat den ”arktiska”, ”svenska” och ”Uppsala”-mutationen.
"”Uppsala” mutationen är något helt nytt som vi påvisat i ett forskningsprojekt med drygt 100 patienter. Mutationen orsakar en aggressiv sjukdom – många bärare insjuknar redan i 40-årsåldern. Vi har upptäckt ytterligare två nya mutationer i kända gener och det finns möjlighet att upptäcka fler i nya gener", säger Vilmantas Giedraitis och berättar att det är forskningen inom just genmutationer som bidragit till ett av de största genombrotten på läkemedelssidan. I slutet av 1990-talet upptäckte professor Lars Lannfelt den ”arktiska” mutationen som har lett till det nya läkemedlet Lecanemab – en antikropp som utvecklats för att minska mängden skadlig amyloid beta i hjärnan. Läkemedlet godkändes nyligen av den amerikanska läkemedelsmyndigheten FDA.
Med hjälp av anslaget från Alzheimerfonden kan nu Vilmantas Giedraitis och hans forskarteam, i samarbete med Akademiska sjukhuset, gå vidare och studera fler patienter.
"Om vi upptäcker nya mutationer kan vi karaktärisera dem och förstå varför de leder till Alzheimers sjukdom. Vi försöker förstå vad som är skillnaden, varför personer med olika mutationer får olika effekter på cellulär nivå och olika sjukdomsförlopp. Vissa mutationer ger till exempel inte bara minnesproblem utan kan också orsaka blödningar i hjärnan. Om vi förstår mekanismerna bakom kan vi behandla med antikroppar eller hitta andra behandlingar."
"Det ligger långt fram i tiden. Men det finns många möjligheter", säger Vilmantas Giedraitis.
Vad hoppas du uppnå med din forskning?
"Jag hoppas att den kan leda till bättre förståelse av sjukdomen och olika former av sjukdomen. Varför får en person sjukdomen vid 50 års ålder, en annan vid 70 och en tredje vid 90 års ålder? Det är ett så stort spektrum. Om vi kan medverka till att sjukdomen bryter ut senare livet eller inte bryter ut alls skulle det vara en stor framgång."

Caroline Graff
Caroline Graff, professor vid Karolinska institutet
Caroline Graff, professor i genetisk demensforskning vid Karolinska institutet, är en av de forskare Alzheimerfonden stöttat under flera år. Nu vill hon göra skillnad för människor som lider av genetiska former av Frontotemporal demenssjukdom, ALS och Alzheimers sjukdom.
"Patienter med frontotemporal demenssjukdom är den grupp som har det allra sämst. De har inte minnesproblem och fångas inte upp av minnestester, de har ofta beteendeförändringar vilka kan tolkas som psykisk sjukdom. I de flesta fall tar det många år innan de får en diagnos vilket orsakar ett stort lidande."
Caroline Graff, professor inom genetisk demensforskning vid institutionen för neurobiologi, vårdvetenskap och samhälle på KI, talar med stark inlevelse om en av de patientgrupper hon ägnar sin forskning åt. Det som skiljer henne från många andra forskare är att hon arbetar kliniskt med patienter och även gör ”grovjobbet”. Den dag vi träffas på hennes arbetsplats Bioclinicum vid Karolinska institutet (KI) i Solna väntar 20 000 prover i labbets frys på att inventeras.
Proverna i labbet kommer från personer med genetiska former av frontotemporal demenssjukdom (FTD) och Alzheimers sjukdom. De genetiska mutationerna är mycket ovanliga och gör att sjukdomarna drabbar dessa personer tidigare i livet och har ett allvarligare förlopp. Cirka 70 personer i vardera gruppen deltar i två stora studier som Caroline och hennes team nu arbetar med. Deltagarna kommer regelbundet till Karolinska Universitetssjukhuset, där de blir undersökta med magnetröntgen och EEG, får göra olika sorters kognitiva tester som MoCA och Eyetracking, lämna blodprover och ta ryggvätskeprov.
"Vad händer med patienter som har den här mutationen tjugo år innan sjukdomen bryter ut? Vi samlar på oss data med målet att i framtiden kunna tillhandahålla genspecifik förebyggande terapi och behandlingar", säger Caroline Graff och fortsätter:
"Vården tar inte hand om de här personerna så våra studier är en form av trygghet för dem. En stor lycka är att vi delar våra resultat med 45 andra forskargrupper i Europa och Kanada i nätverket Genfi. Det är så vi måste jobba med sällsynta sjukdomar. Det vi skapar här kommer till nytta för många familjer och gör att våra deltagare känner sig mindre ensamma."
Frontotemporal demenssjukdom (FTD) manifesteras inte genom minnesproblem utan genom sociala, beteendemässiga och/eller språkliga störningar. Det gör patientgruppen svår att fånga upp inom vården och skapar oerhört lidande för patienter och anhöriga. Symtom hos den som lider av sjukdomen kan bland annat vara att man isolerar sig, förändrar sitt beteende mot anhöriga, drabbas av samlarmani och tar ekonomiskt oöverlagda beslut.
"Inom vården är man ovan att diagnosticera den här gruppen och vågar inte riktigt eftersom de inte har minnesproblem. Inte ens på en minnesmottagning har man som rutin att fråga efter beteendeförändringar. En av våra utmaningar är att försöka hitta metoder för att mäta social kognition", säger Caroline Graff.
Ett viktigt mål i hennes forskningsprojekt är att utveckla biomarkörer för att kunna ställa tidig diagnos och förutspå sjukdomsutvecklingen. För Alzheimers sjukdom finns idag mycket bra diagnostiska verktyg - biomarkörer både i ryggvätska och blod. För frontotemporal demenssjukdom, där så många som en femtedel av sjukdomsfallen beror på en mutation, saknas det helt.
Caroline berättar att proteinet TDP-43 ses som en möjlig biomarkör för frontotemporal demenssjukdom (FTD), men även för den allvarliga neurodegenerativa sjukdomen amytrofisk lateralskleros (ALS).
Sjukdomen ALS, som de flesta av oss kopplar ihop med gradvisa nedbrytning av nervceller och muskelförtvining, har en stark koppling till FTD. Genen C9orf72 är nämligen den vanligaste genetiska orsaken både till FTD och ALS. Och den senaste forskningen stödjer uppfattningen att båda sjukdomarna tillhör samma spektrum och överlappar varandra. Patienter med ALS har ofta precis som personer med FTD en kemisk obalans i hjärnan och uppvisar beteendeförändringar.
"Hälften av alla ALS-patienter har en kognitiv beteendepåverkan. Men varför hanteras dessa patientgrupper så olika inom vården och varför är forskningsområdena helt isolerade från varandra? Det är vansinne. Här på KI har vi startat ett interdisciplinärt forskningsnätverk som syftar till att integrera forskning om de båda sjukdomarna och hoppas att det ska leda till förbättringar för dessa patienter."
Vad betyder anslaget 850 000 kronor från Alzeimerfonden för dig?
"Anslaget betyder självklart jättemycket för oss. Den forskning vi bedriver är mycket kostsam. Vi beräknar till exempel att varje studiebesök, då en deltagare besöker oss och genomgår magnetröntgen, kostar 30 000 kronor."

Martin Hallbeck, biträdande professor, Linköpings Universitet
Martin Hallbeck, biträdande professor och verksamhetschef klinisk patologi vid Universitetssjukhuset i Linköping, har länge studerat de processer i hjärnan som orsakar Alzheimers sjukdom. 2020 tilldelades han ett forskningsanslag på 1,75 miljoner kronor från Alzheimerfonden.
Forskare inom Alzheimerfältet har på senare tid blivit allt mer säkra på att det är intracellulära ansamlingar av felveckade proteinaggregat av beta-amyloid som till stor del är drivkraften och orsaken till att cellerna bryts ner och gör att sjukdomen bryter ut. De senaste åren har Martin Hallbeck och hans forskargrupp kunnat visa hur sådana ansamlingar av felveckade proteinaggregat sprids mellan celler i hjärnan. Något som kan förklara varför patienter gradvis blir allt sjukare när mer och mer av hjärnan drabbas. En viktig spelare tycks vara de exosomer, pyttesmå blåsor, aggregaten kan tjuvåka på från cell till cell, från ett hjärnområde till ett annat. Exosomernas last av aggregat fungerar sedan som katalysatorer så att nya aggregat bildas och nya celler blir sjuka.
Ett annat fokusområde för Martin Hallbecks forskning kring spridningen av Alzheimers är så kallade gap junctions, en sorts kopplingar mellan nervcellerna som gör att de kan prata med varandra. Väggarna i de små kanalerna mellan nervcellerna byggs upp av proteiner som regelbundet byts ut. Då passar de giftiga aggregaten av beta-amyloid på att samtidigt smita in i cellen.
"Vi vill också förstå varför cellerna inte bryter ned de giftiga proteinaggregaten när de tar sig in i cellerna. Hos patienter med Alzheimers sjukdom är cellnedbrytningssystemet försämrat i sin funktion vilket bidrar till ansamling av proteinaggregat. Vi tror också att det leder till att mer beta-amyloid hamnar i exosomerna och att spridningen av sjukdomen därmed går snabbare. Om vi kan visa och förstå hur de här mekanismerna fungerar kan vi också angripa processerna och stoppa spridningen av sjukdomen", säger Martin Hallbeck.
Vad kan din forskning göra för nytta för alzheimerpatienterna?
"Vi testar olika substanser och försöker också utveckla egna substanser som kan bromsa spridningen, vilket jag på lång sikt tror kan leda till behandlingar. Om vi förstår hur spridningen av sjukdomen går till kan kunskaperna också användas inom diagnostiken och för att förutsäga hur snabbt ett sjukdomsförlopp riskerar att bli. Vårt mål är att kunna bidra både inom diagnostik och behandling."
Vad betyder forskningsanslaget från Alzheimerfonden på 1,75 miljoner?
"Det betyder att vi kan vara fler som arbetar och att vi kan gå fortare fram. Pengarna gör att vi kan arbeta med mer avancerade verktyg. Anslaget är dessutom en viktig kvalitetsstämpel för vår forskning och gör det lättare för oss att samarbeta med de forskare vi vill samarbeta med."

Greta Hultqvist, biträdande lektor, Uppsala Universitet
Greta Hultqvist, docent och universitetslektor vid Institutionen för farmaci vid Uppsala universitet, har 2021 tilldelats 700 000 kronor i forskningsbidrag från Alzheimerfonden.
"Jag är jättestolt och glad. Alzheimerfonden var den första organisation som vågade satsa på mig redan som ung och nydisputerad forskare och har beviljat mig stöd under många år. Det ger mig en enorm trygghet att våga satsa på min forskning och är essentiellt för att jag ska kunna fortsätta". säger Greta Hultqvist.
Hon är en av de forskare som arbetar med att angripa Alzheimers sjukdom med det som kallas immunterapi det vill säga en behandlingsform som går ut på att trimma kroppens egna celler så att de orkar fungera som vanligt. Hos patienter med Alzheimers sjukdom handlar det om att försöka aktivera hjärnans egna mekanismer för att bryta ner aggregaten eller klumparna av proteinet amyloid-beta som bildas i hjärnan och drabbar patientens kognitiva förmåga. Än så länge utförs all forskning på möss.
"Det fantastiska är att vi har lyckats förstärka kroppens eget sätt att bryta ner de skadliga aggregaten. Med hjälp av ett hjärntransportör-protein kan vi skicka in kroppens egen peptid somatostatin i hjärnan, ett hormon som förstärker kroppens egen förmåga att bryta ner de skadliga aggregaten. Vi ser då att nedbrytningen uppregleras så att nivåerna av amyloid-beta liknar den hos friska individer."
En av svårigheterna med immunterapi är den så kallade blod-hjärnbarriären som hindrar giftiga ämnen att passera in i hjärnan men även antikroppar som skulle kunna hjälpa till i städningsarbetet. Ett viktigt fokus för Greta Hultqvists forskningsteam är utveckla bättre hjärntransportör-protein som kan öka upptaget av antikropparna i hjärnan men även se till att de blir kvar länge och kan utföra sitt arbete.
Ett annat viktigt mål är att utveckla nya och effektiva antikroppar som kan binda till och bryta ner de stora aggregaten av amyloid-beta men även de mindre som idag anses vara de farligaste för nervcellerna.
"Strategin är att bryta ner amyloid-beta innan den börjar aggregera. Det är när det bildas för mycket som det börjar klumpa ihop sig och blir skadligt."
Vad kan din forskning göra för nytta för alzheimerpatienterna?
"Mitt mål är att den ska kunna leda till framtida behandlingar. Med nya proteinläkemedel tror jag absolut att vi kan öka nedbrytningen av amyloid-beta –byggstenarna bakom aggregaten. Vi kommer inte att kunna reversera sjukdomen men se till att den inte förvärras. Om den upptäcks i tid kan det göra stor skillnad."

Martin Ingelsson, docent, Uppsala universitet
Alzheimerfonden stöttar Martin Ingelssons intressanta forskning kring den genetiska kopplingen till Alzheimers sjukdom.
Du studerar vilka genetiska förändringar som ökar risken för demenssjukdomar. Hur går dessa studier till?
"På flera olika sätt. Vi undersöker förekomsten av mutationer, som var och en för sig leder till sjukdom, ofta med en insjuknandeålder under 65 år. Dessutom genomför vi tillsammans med andra forskargrupper stora studier, i vilka vi samlar tusentals DNA-prover från friska och sjuka för att undersöka förekomsten av s.k. sårbarhetsgener. Bärare av specifika förändringar i dessa gener har en viss ökad risk att insjukna och denna risk kan förväntas öka ju fler sådana förändringar man bär på."
Vad har ni kunnat dra för slutsatser hittills?
"Att mutationer i någon av de tre alzheimergenerna – APP, PS1, PS2 – tack och lov är relativt sällsynta (< 1% av alla sjukdomsfall). Bärarskap av en eller flera genetiska riskvarianter är betydligt vanligare. Dock är riskökningen inte så stor för dessa, åtminstone inte när man tittar på var och en för sig. Undantaget utgörs av den s.k. APOE-genen, där personer med E4-varianten faktiskt löper 3-10 ggr större risk att insjukna jämfört med dem som bär på antingen E2 eller E3."
Är det vanligare med genetiskt betingad demens i familjer där sjukdomen brutit ut i yngre år?
"Ja, oftast är det så. I dessa fall debuterar sjukdomen vanligtvis redan i 50–65 årsåldern och i sällsynta fall redan vid 40 års ålder eller ännu tidigare. I vissa fall kan dock vissa av våra patienter insjukna före 65 år även då ingen ärftlighet tycks föreligga. Dock kan ärftligheten vara svår att få korrekt information om. Till exempel kan föräldrarna ha avlidit tidigt av andra orsaker."
Är sjukdomsförloppet annorlunda vid genetisk demens?
"Sjukdomen är ibland mer aggressiv när det finns en stark underliggande genetik, men detta behöver inte vara fallet. Det är inte heller så att samma genetiska förändring alltid ger samma sjukdomsbild; både insjuknandeåldern och den tid sjukdomen pågår kan skilja sig så mycket som 10–20 år mellan två patienter som bär på samma alzheimermutation."
Vilket råd skulle du ge unga människor med föräldrar som drabbats i yngre år?
"Att ta kontakt med den mottagning som skött utredning och behandling av föräldern. Den ansvariga läkaren kan svara på frågor om sjukdomen, hur stor risken är att sjukdomen går i arv och vad man ska tänka på som anhörig. Om man inte får information som man är nöjd med kan man också vända sig till de centra i landet som har ett speciellt intresse av dessa frågor, till exempel vid Akademiska sjukhuset i Uppsala eller Huddinge sjukhus."
Varför drabbas nästan alla personer med Downs syndrom av Alzheimers sjukdom?
"Det beror på att personer med Downs syndrom har en extra kopia av den gen, APP, som leder till att proteinet beta-amyloid bildas. I deras hjärnor bildas helt enkelt för mycket beta-amyloid, som inte kan transporteras bort utan inlagras mellan nervcellerna och bildar s.k. plack. Konsekvensen blir att kommunikationen mellan cellerna störs och att de så småningom dör."
Hur många olika grupper av genmutationer finns det?
"I de tre alzheimergenerna finns totalt knappt 200 olika mutationer. Flest finns för PS1-genen (mer än 150), medan mutationer i APP (cirka 35) och PS2 (drygt 10) är mer ovanliga."
Vad hoppas du att din forskning ska leda till i framtiden?
"Förutom att fortsätta kartlägga genetiken, och därmed öka förståelsen för sjukdomsmekanismerna, försöker vi omsätta kunskapen för att hitta nya sätt att ställa diagnos och utveckla mer effektiva läkemedel. Vi är den enda forskargrupp i landet som tagit fram en behandling från idé till klinisk prövning för Alzheimers sjukdom. Antikroppar mot giftiga former, s.k. protofibriller, av beta-amyloid utvärderas nu på ett stort antal patienter i både USA och Europa. Vidare bedriver vi forskning kring Parkinsons sjukdom och även där tror vi att behandling med antikroppar mot protofibriller av alfa-synuklein, det protein som förefaller orsaka sjukdomsprocessen, i framtiden kan komma att prövas på patienter. Våra behandlingsförsök på en musmodell för sjukdomen har gett lovande resultat."

Shorena Janelidze
Shorena Janelidze, forskare vid Lunds universitet
Shorena Janelidze, forskare vid avdelningen för Klinisk minnesforskning vid Lunds universitet, har tilldelats 1,3 miljoner kronor av Alzheimerfonden. Syftet med hennes projekt är att hitta nya biomarkörer, som kan förbättra diagnostiken av neurodegenerativa sjukdomar, men även att identifiera nya läkemedelskandidater, som i förlängningen kan leda fram till nya sjukdomsmodifierande terapier.
"Det är mycket uppmuntrande att få ett så stort anslag. Det gör att jag själv kan arbeta mer effektivt i projektet och även koppla in fler medarbetare", säger Shorena Janelidze, när vi ses på hennes arbetsplats i Lund där hon har arbetat i mer än tjugo år.
I dag finns bra verktyg för att diagnosticera Alzheimers sjukdom i ryggvätske- och blodprov med hjälp av så kallade biomarkörer medan många andra neurodegenerativa sjukdomar är svåra att diagnostisera. Glädjande nog finns nu en godkänd behandling för Alzheimers sjukdom, som dock endast måttligt bromsar den kognitiva nedgången hos patienter, men för närvarande inga sjukdomsmodifierande terapier för andra neurodegenerativa sjukdomar.
För att utveckla nya och effektiva läkemedel behöver forskarna bättre förstå mekanismerna bakom olika neurodegenerativa sjukdomar inklusive Alzheimers sjukdom. Detta är särskilt viktigt eftersom många patienter som har Alzheimers sjukdom även har andra sjukliga förändringar i hjärnan, ansamlingar av proteiner, som kan ge upphov till sjukdomar som Lewykroppsdemens och LATE (Limbic-predominant age-associated TDP-43 encephalopathy).
"Det är mycket glädjande och ett stort genombrott att vi har fått de första bromsmedicinerna som Leqembi, men det räcker inte med läkemedel som riktar sig mot amyloid-beta. För att förbättra och snabba upp utvecklingen av nya läkemedel måste vi få en bättre förståelse för till exempel vilka proteiner som är inblandade i aggregeringen och spridningen av amyloid-beta och tau och vad som ”triggar igång” aggregeringen", säger Shorena Janelidze.
För att komma närmare svaret på den frågan kommer Shorena och hennes team att använda ryggvätskeprover från tusentals personer i olika länder bland annat USA, Danmark, Tyskland, Spanien, Italien och Sverige, som finns samlade i ett internationellt konsortium. Prover från 6 000 deltagare som lever med neurodegenerativa sjukdomar som Alzheimers sjukdom, Parkinsons sjukdom, och även mindre vanliga sjukdomar som Lewykroppsdemens, Frontotemporal demens och Amyotrofisk lateralskleros men även friska kontrollpersoner kommer att undersökas. Med hjälp av proteomik, en metod för att studera proteiner, kan man mäta 5 400 olika proteiner i ett och samma prov.
"Vi genererar enorma mängder data som det kommer att ta tid att analysera innan vi kan publicera våra resultat", säger Shorena Janelidze och fortsätter:
"Vår förhoppning är att hitta de biologiska mekanismer som ligger bakom de olika sjukdomarna. Vad har de gemensamt? Vad är unikt för varje sjukdom? Målet är att hitta nya biomarkörer för de olika neurodegenerativa sjukdomarna och identifiera nya läkemedelskandidater."
Ännu ett syfte med projektet är att hitta nya verktyg för att bättre kunna förutsäga sjukdomsförloppet hos enskilda patienter. Här använder Shorena och hennes team ryggvätske- och blodplasmaprover från deltagare i de svenska BioFinder1- och BioFinder2-studierna. Mer än 12 000 prover kommer att analyseras med NULISA-proteomik specifikt inriktat på proteinerna i det centrala nervsystemet.
"Här kommer vi studera prover tagna vartannat år i upp till åtta års tid. Vi hoppas våra resultat kommer att förbättra möjligheterna att förutsäga hur Alzheimers sjukdom men även andra neurodegenerativa sjukdomar utvecklas över tid."

Miia Kivipelto Foto: Bruno Ehrs
Miia Kivipelto, professor, Karolinska Institutet
Miia Kivipelto, är professor vid Karolinska Institutet och forskningschef på Tema Åldrande, Karolinska Universitetssjukhuset. Hon är också kvinnan bakom den mycket uppmärksammade svensk-finska FINGER-studien. Den första studien i världen som visar att det går att förebygga minnesstörningar med hjälp av en hälsosam livsstil. Vi har ställt några frågor till henne.
När resultaten från Finger-studien publicerades 2015 blev uppmärksamheten stor. Studien visade att man med regelbunden fysisk aktivitet, kosthållning, minnesträning och hantering av blod-kärlrelaterade riskfaktorer kan påverka risken att utveckla minnesbesvär och kognitiv svikt.
Vad har studien lett till?
"Intresset från omvärlden har varit enormt. 2017 startade vi nätverket – World Wide FINGERs – där 30 länder medverkar. Nästan varje dag har jag Skype-samtal med deltagande forskare runt om i världen. I våras blev Finger-modellen vägledande för WHO:s riktlinjer när det gäller att förebygga demenssjukdomar. Förra året startade vi även FINGERS Brain Health Institute i Stockholm bland annat med stöd från Alzheimerfonden – en ny plattform för att implementera det förebyggande arbetet mot demenssjukdomar", berättar Miia Kivipelto och fortsätter:
"Vi jobbar mycket aktivt med att föra ut våra forskningsrön till minnesmottagningarna. Vi arbetar bland annat med Kognitiv mottagning vid Karolinska Universitetssjukhuset i Solna där medelåldern hos patienterna är 58 år. Vi försöker att paketera råden i Finger-modellen mer tydligt och hitta sätt att individanpassa och skräddarsy paketen efter patientens riskprofil. Vi tar bland annat hjälp av ny teknik som appar för att ge extra stöd."
Vad har du för råd till unga människor som lever nära en anhörig med en demenssjukdom?
"När en nära anhörig får en demenssjukdom är det väldigt mycket känslor och stress. Det är mycket viktigt att de unga tar hand om sig själva och sin hälsa, att de hittar stunder att bara tänka på sig själva."
Hur kan de unga anhöriga hjälpa sina nära och kära som har fått en demenssjukdom?
"I vår studie MIND-AD, där deltagarna nyligen fått sin alzheimerdiagnos, har vi använt en anpassad FINGER-modell och sett fantastiska resultat. Även om man har fått en diagnos är det inte för sent att göra något. Efter ett besked är det lätt att hamna i ett tomrum och tappa orienteringen. Men det går att ta kommandot – förbättra sin fysik, orka mer och lära sig nya saker. Det är viktigt att vara fysiskt aktiv på gymmet, hemma eller ute naturen med sina anhöriga och med vänner. Vi rekommenderar mångsidig träning – både muskelstyrka och balansträning och gärna i grupp så att man träffar andra och kan byta tankar och erfarenheter. Tidigt i sjukdomen är det ganska vanligt att man går ner i vikt. Det är viktigt att äta en mångsidig, hälsosam och balanserad kost och att träna hjärnan genom att läsa och vara aktiv. I MIND-AD använde vi ett databaserat träningsprogram där man tränar minnet och hur man kan hantera vardagliga situationer. Självklart är det också viktigt att hålla koll på riskfaktorer som blodtryck, kolesterol och diabetes och att optimera sin medicinering. Och att tänka på att hjärnan dessutom behöver vila och koppla av."
Hur tror du att framtidens behandlingar mot demenssjukdomar kommer att se ut?
"Det har varit svårt att hitta nya läkemedel, men just nu ser vi några positiva signaler i nya läkemedelsstudier. Nu testas även andra typer av läkemedel inte bara mot betaamyloid utan även mot tau och inflammationer. Redan nästa år hoppas jag att vi kan börja med en studie där man testar metformin, ett läkemedel som används mot diabetes men som har visat sig att kunna minska risken för Alzheimers sjukdom. Jag tror kombinationen av förebyggande FINGER-baserade livsstilsåtgärder och olika läkemedel kommer att vara framtidens melodi."
Fakta FINGER
FINGER-studien är den första interventionsstudien i världen som visar att det går att förebygga minnesstörningar. Studien visar att kostråd, fysisk träning och kognitiv träning samt kontroll av vaskulära riskfaktorer som högt blodtryck, blodsocker och blodfetter har positiv betydelse för hjärnan.

Sara Linse
Sara Linse, professor vid Lunds universitet
Sara Linse, professor i fysikalisk kemi vid Lunds universitet, har tilldelats nära 1,2 miljoner kronor av Alzheimerfonden. Syftet är att undersöka möjligheten att ”härma” kroppens eget naturliga försvar mot att amyloida plack och tau-fibriller bildas i hjärnan.
90 000. Så många olika slags proteiner produceras uppskattningsvis i våra kroppar. Nära en femtedel på viktbasis är så kallade chaperoner eller stödjeproteiner, som ser till att våra proteiner inte veckas fel eller klumpar ihop sig. Sedan tidigare vet forskarna att en grupp chaperoner utgör ett naturligt försvar mot amyloidsjukdomar som Alzheimers sjukdom. Dessa chaperoner arbetar på två sätt – de förhindrar bildandet av de amyloida placken men kan även lösa upp existerande plack.
"Vi vill försöka förstå vilka delar av chaperonen som bidrar till att det har den här effekten. Och med den kunskapen försöka skapa något liknande, en kopia eller en mindre molekyl som arbetar på samma sätt", säger Sara Linse och fortsätter:
"Förhoppningen är att vi kan lära oss så mycket att det så småningom kan leda till att vi får fram läkemedelsmolekyler med samma lösande effekt som chaperonerna, eller behandlingar som kan boosta kroppens chaperoner."
Sara Linses forskningsteam kommer specifikt att kartlägga chaperonet med benämningen DNAJB6 och undersöka vilken effekt det har på proteinerna beta-amyloid och tau, som båda är starkt kopplade till utvecklingen av Alzheimers sjukdom.
"Vi kommer att undersöka hur olika varianter och olika halter av chaperonen påverkar och förändrar proteinerna. Det är en stor molekyl – kan vi skala ner den? Vad kan vi ta bort, vad måste finnas kvar? Målet är att hitta det minsta verksamma elementet", säger Sara Linse.
I arbetet kombinerar forskarna många tekniker, bland annat superupplösande mikroskopi, spektroskopi och kärnmagnetisk resonans. Något av det viktigaste i den komplicerade processen är reningen av proteinerna som sker med hjälp av ultraljudsbehandling och jonbytes- och gelfiltreringskromatografi.
"Vårt lab har stark kompetens i att rena protein. Men jag tror att vår största styrka är vår metodologi – att tänka på varje steg och kombinera metoder till en helhet så att hela experimentkedjan fungerar."
Vad betyder anslaget från Alzheimerfonden för ditt forskningsprojekt?
"Det känns fantastiskt att få så stort anslag. Det innebär att vi får fler händer i labbet, att vi kan anställa en person som kan jobba med detta, det är väldigt generöst."

Francesca Mangialasche, biträdande lektor, Karolinska Institutet
Francesca Mangialasche, assistant professor vid Karolinska Institutets avdelning neurobiologi, vårdvetenskap och samhälle, specialist i geriatrik och vetenskaplig koordinator för nätverket World Wide FINGERS har 2020 tilldelats 1,2 miljoner i forskningsbidrag från Alzheimerfonden:
"Jag är så glad. Det är en stor ära och ett stort personligt erkännande men också ett kvitto på att forskningen kring prevention av Alzheimers sjukdom är på frammarsch".
FINGER-studien med 1260 deltagare i åldern 60-77 var den första multimodala interventionsstudien i världen som visade att kostråd, fysisk och kognitiv träning, social stimulering samt kontroll av vaskulära riskfaktorer under två års tid kan förebygga kognitiv försämring i hjärnan.
2017 startades det globala nätverket World Wide FINGERS där idag cirka 35 länder medverkar. Som vetenskaplig koordinator är Francesca Mangialasche mycket involverad i arbetet med att implementera den FINGER preventiva modellen runt om i världen för att förebygga demenssjukdomar.
Sedan FINGER-studien startade 2009 har deltagarna med jämna intervaller i upp till tio år lämnat blodprover. Dessa blodprover är nu grunden i det projekt Francesca Mangialasche har beviljats pengar för. Genom att studera nya biomarkörer i blodet kopplade till Alzheimers sjukdom i de blodprover som lämnats genom åren kan forskarna se hur förändringarna över tid korrelerar mot förändringar i kognitiva funktioner och utvecklingen av sjukliga förändringar i hjärnan. Biomarkörerna gör det möjligt för forskarna att identifiera de personer som kan ha störst nytta av preventiva åtgärder.
”Har alla deltagare tack vare vår prevention förebyggt en kognitiv försämring på lång sikt? Fungerar det bättre på vissa patienter? Hur kan vi i så fall identifiera patienter som har största nytta av FINGER-modellen", säger Francesca Mangialasche.
För att ställa diagnosen Alzheimers sjukdom behöver man idag ta prov från ryggvätskan, som också kallas cerebrospinalvätskan, eller göra dyrbara PET-undersökningar av hjärnan. Att i framtiden kunna följa sjukdomsförloppen genom ett nytt enkelt blodprov skulle göra det möjligt att rulla ut den preventiva FINGER-modellen i stor skala.
"Målet är att skapa skräddarsydda preventionsmetoder där vi arbetar med biomarkörer och med livsstilsfaktorer som kan användas i hela världen. Hittar vi personer med risk för demens i god tid kan vi fördröja de kognitiva problemen och se till att de insjuknar så sent som möjligt eller förhoppningsvis inte alls."

Anna Matton
Anna Matton, docent vid Karolinska institutet
FINGER-studien var först i världen att visa att det går att förebygga minnesstörningar med hjälp av en hälsosam livsstil. Anna Matton, forskare vid Karolinska institutet, testar en liknande modell på möss för att komma närmare svaret på hur vi kan förebygga Alzheimers sjukdom och i framtiden skräddarsy behandlingar.
År 2024 tilldelades Anna Matton, docent vid Institutionen för neurobiologi, vårdvetenskap och samhälle vid Karolinska institutet, ett anslag på 850 000 kronor från Alzheimerfonden
"Det är enormt betydelsefullt. Utan anslaget skulle vi inte kunna bedriva vår grundläggande forskning och bygga upp en egen biobank, en plattform som kommer att kunna användas i många nya projekt. För mig personligen betyder stödet mycket, jag får tillfälle att utveckla min egen forskningslinje", säger Anna Matton när vi ses på hennes arbetsplats Bioclinicum på Karolinska institutet.
Anna Matton arbetar tillsammans med professor Miia Kivipelto som driver den omtalade FINGER-studien. Den har visat att regelbunden fysisk aktivitet, kosthållning, minnesträning och hantering av blod-kärlrelaterade riskfaktorer kan påverka risken att utveckla minnesbesvär och kognitiv svikt. I sitt eget forskningsprojekt på möss, som hon driver tillsammans med andra forskare på avdelningen, går hon vidare för att söka svar på vad som fungerar bäst – att arbeta förebyggande med livsstilsfaktorer, att använda läkemedel eller en kombination av båda.
"Alzheimers sjukdom är en heterogen sjukdom. Vi måste få en bättre förståelse på molekylär nivå varför vissa saker fungerar och förbättrar kognitionen. Det är nyckeln för att i framtiden kunna utveckla preventionsprotokoll och även läkemedel som genom precisionsmedicin kan skräddarsys för att passa olika grupper", säger Anna Matton.
För att bättre förstår vilka vägar som utlöser kognitiva vinster arbetar Anna Matton och hennes team med musmodeller. I en unik modell har de undersökt hur kognitionen hos tre ”sorters” möss, (en med ett prekliniskt stadium av Alzheimers, en med en vaskulär demens samt en kontrollgrupp), påverkas av livsstilsfaktorer respektive läkemedel. I den så kallade livsstilsgruppen har mössen fått både fysisk och kognitiv träning i ett eget konstruerat Intellicage-system samt matats med ett specifikt kosttillskott. I läkemedelsgruppen har mössen fått blodtrycks- och kolesterolsänkande medicin, medan kontrollgruppen fått en vanlig diet. I modellen ingår även blodprovstagning, blodtrycksmätning och olika tester för att mäta kognitionen. Resultaten sammanfattas nu i en avhandling av doktorand Vilma Alanko.
"Om jag ska försöka sammanfatta våra resultat från de tre grupperna är det tydligt att livsstilsprevention har en effekt på kognitionen och hjärnan, men de molekylära mekanismerna som aktiveras skiljer sig åt mellan olika musmodeller. Jag tror att det här är framtiden – att arbeta både med livsstil och med läkemedel – blanda för att få bästa möjliga effekt i varje individ", säger Anna Matton.
Hjärnvävnaden från de olika testgrupperna har dissekerats och analyserats med hjälp av proteomik (tusentals protein) och lipdomik (olika fetter och fettliknande molekyler).
"Målet är att få en bättre förståelse för vilka mekanismer som bidrar till att kognitionen förbättras. Vi är inte där ännu men vi vill bidra till att i framtiden hitta behandlingar som kan skräddarsys för patienter med olika varianter av sjukdomen."

Wojciech Michno
Wojciech Michno, biträdande universitetslektor vid Uppsala universitet
Wojciech Michno, biträdande universitetslektor vid Uppsala universitet, har tilldelats 1,2 miljoner till ett projekt som undersöker möjligheten att förbättra behandlingar med antikroppsbaserade läkemedel och göra dem säkrare.
Innan det blev ett ja sa Europeiska läkemedelsmyndigheten (EMA) först nej till att godkänna bromsmedicinen Lecanemab med hänvisning till flera fall där patienter drabbats av komplikationer som ödem och mikroblödningar. Den neuroinflammation som kan uppstå i hjärnan hos vissa patienter vid behandling är dåligt genomlyst. Här krävs mer forskning för att i framtiden kunna identifiera patienter som riskerar att få biverkningar och bara en begränsad effekt av behandlingen.
"Vi måste bli bättre på att förstå hur antikroppsbehandlingarna påverkar cellerna i specifika regioner för att förebygga biverkningar och göra behandlingen bättre", säger Wojciech Michno.
I projektet som han och hans team fått anslag för studerar de bland annat hur immunsystemet och cellulära mikromiljöer hos musmodeller av Alzheimers sjukdom påverkas på kort och lång sikt av antikroppsbehandlingarna. Med hjälp av masspektrometribaserad molekylär avbildning (IMS) kan de se hur små byggstenar som lipider (en stor grupp ämnen bestående av fetter och fettliknande ämnen), peptider och glykaner reagerar på behandlingarna. De kombinerar det med genetiska analyser, och fokuserar på både själva hjärnan och det vaskulära systemet.
"Vi tror starkt att lipider kan vara en viktig pusselbit för att förstå inflammationen i hjärnan vid Alzheimers sjukdom. De kan ge insikt i vilka biologiska processer som pågår och vissa lipider kan ha potential att utvecklas till biomarkörer för sjukdomen."
Wojciech Michno och hans team intresserar sig också för hjärnans eget immunsystem. Kan det hjälpa till att förhindra den inflammation som uppstår i hjärnan vid Alzheimers sjukdom eller kan det tvärtom förvärra den?
"Vi studerar om effekterna av att nedreglera eller uppreglera immunsystemet. Vi måste se vad vi kan göra för att motverka sjukdomsförloppet. I framtiden kommer vi möjligen kombinera antikroppsbehandlingar med immunmodulerande behandlingar, kanske även genom att modifiera en och samma antikropp. Vi hoppas att våra data kan bidra till det och vara nyckeln till att göra behandlingarna mer effektiva."
Vad betyder anslaget från Alzheimerfonden för dig?
"Våra analyser är mycket kostsamma, så det är mycket glädjande att få anslaget och det visar att fler än jag och min grupp anser att vårt projekt är viktigt. Alzheimerfonden har mycket kompetenta personer i sitt vetenskapliga råd som satsar brett på olika forskningsområden. Det bidrar till att forskningen går snabbare framåt."

Laia Montoliu-Gaya
Laia Montoliu-Gaya, forskare vid Göteborgs universitet
Med nya lovande bromsmediciner mot Alzheimers sjukdom ökar behovet av effektiva diagnostiska verktyg för att kunna sätta in behandlingar i tid. Laia Montoliu-Gaya, forskare vid Göteborgs universitet, hoppas kunna ta fram ett nytt sorts blodprov, möjligt att skicka in per post, som kan visa var i sjukdomsförloppet en person befinner sig.
2024 tilldelades Laia Montoliu-Gaya, forskare vid sektionen för psykiatri och neurokemi vid Göteborgs universitet, ett anslag på 1,3 miljoner kronor av Alzheimerfonden för sitt forskningsprojekt ”Alzheimer’s disease staging from a fingerstick”.
"Jag är mycket glad och tacksam för anslaget. Det gör det möjligt för mig att kombinera två av mina tidigare forskningsprojekt och ta dem vidare. Som relativt ung forskare känns det bra att kunna driva mitt eget projekt självständigt", säger Laia Montoliu-Gaya,
Hon visar runt på sin arbetsplats, laboratoriet som ligger på Mölndals sjukhus och som hon delar med namnkunniga kollegor som Henrik Zetterberg och Kaj Blennow. I olika rum finns det allra senaste inom analystekniken som bland annat används för att mäta alzheimermarkörer i blod och ryggvätska.
Sedan länge anses p-tau-217, vara en mycket lovande alzheimermarkör, som kan påvisa alzheimerpatologi i hjärnan med nästan lika stor träffsäkerhet som ryggvätskeprov och undersökning i PET-kamera. I sin tidigare forskning har Laia Montoliu-Gaya använt en unik masspektrometrimetod som kan kvantifiera flera tau-arter i blod. Hon var tidigt ute med att designa en panel som kan identifiera de tre mest effektiva tau-biomarkörerna för att bedöma var i sjukdomsförloppet en patient befinner sig.
"Vi har valt ut tre olika sorters tau-protein som vi tror är optimala för att berätta i vilket stadie av sjukdomen en person befinner sig. P-tau217 i det tidiga skedet, p-tau205 något längre fram i sjukdomen och 0N tau när sjukdomen brutit ut. Att få en uppfattning om var i sjukdomen en person befinner sig är mycket viktigt när vi har nya terapier som kan sättas in tidigt", säger Laia Montoliu-Gaya.
Nästa steg i projektet har varit att utveckla antikroppar som kan binda till de olika tau-proteinerna. Det görs i samarbete med ett amerikanskt företag men kommer i förlängningen att ske på plats i Mölndal. Att de tre tau-arterna verkligen är optimala markörer vid olika skeden av sjukdomsutvecklingen utvärderas genom ett samarbete med minneskliniker i Sverige och Spanien.
Målet är att utveckla en multiplexanalys som är skräddarsydd för de specificerade tau-markörerna för de olika stadierna av Alzheimers sjukdom. I ett första steg kommer Laia Montoliu-Gaya och hennes forskargrupp testa om analysen fungerar i ett vanligt blodprov. I nästa steg är målet att utveckla ett ”fingerstick test”. Lite enkelt förklarat kan man säga att det är ett test-kit som man kan få hemskickat via en vårdcentral eller liknande instans, göra ett stick i fingret, droppa lite blod på ett kort och sedan skicka per post till ett laboratorium.
"Jag hoppas att det ska fungera som ett ”fingerstick test”. Det är så många patienter som blir feldiagnosticerade idag. Det hade varit en stor hjälp till exempel för personer som bor på otillgängliga platser att enkelt kunna få en första diagnos och därefter bli kallad till en minnesklinik", säger Laia Montoliu-Gaya och berättar att de just nu har sex olika grupper som validerar metoden. Varje vecka kommer det in nya prover som analyseras,
Forskningsprojektet kommer att fortsätta under många år och även innefatta studier av faktorer som kan påverka tau-markörernas tillförlitlighet som till exempel kön, ålder, njurproblem, diabetes och olika livsstilsfaktorer.
"Det kommer vi också att undersöka i samarbete med den stora studien REAL AD som pågår här i Västra Götalandsregionen", avslutar Laia Montoliu-Gaya.
Rik Ossenkoppele
Rik Ossenkoppele, forskare vid Lunds universitet
I september 2021 fick Rik Ossenkoppele, ta emot det prestigefulla ”Drottning Silvias pris till en ung alzheimerforskare” på 125 000 kronor. Vi ställde några frågor till honom.
Varför vill du forska om Alzheimers sjukdom?
"En kombination av aspekter har väckt mitt intresse för att forska om Alzheimers sjukdom. För det första har jag många gånger sett de förödande effekterna Alzheimers sjukdom kan ha på en individ och deras nära och kära. Utan något effektivt botemedel tillgängligt är jag väldigt motiverad att bidra till en lösning. För det andra har jag alltid varit fascinerad av de många ansikten denna sjukdom har, eftersom den manifesterar sig så olika mellan individer. Att förstå orsakerna till dessa individuella skillnader kan vara nyckeln till att lösa Alzheimers sjukdom. För det tredje kännetecknas Alzheimers sjukdom av en ganska gradvis nedgång, eftersom de flesta individer tillbringar mer tid i den asymtomatiska fasen (där den biologiska sjukdomsprocessen redan har börjat, men inga tydliga symtom har dykt upp ännu) än i den symtomatiska fasen. Detta ger en stor möjlighet att stoppa Alzheimers sjukdom innan den bryter ut. För det fjärde, den första beskrivningen av Alzheimers sjukdom går tillbaka till 1906 och vi har fortfarande inte hittat en tillfredsställande lösning. Jag känner mig mycket personligen utmanad av Alzheimers sjukdoms komplexa natur."
Vad är syftet med din forskning?
"Mitt forskningsprogram har tre olika syften. Den första är att förstå rollen av de två centrala patologiska kännetecknen för Alzheimers sjukdom (dvs amyloida plack och tau-fibriller) i uppkomsten och progressionen av Alzheimers sjukdom. Vi mäter dessa patologier med hjälp av PET-skanning och relaterar dessa processer till förändringar i kognition, förlust av hjärnceller och hjärnfunktion. För det andra studerar vi skillnaderna i klinisk presentation vid Alzheimers sjukdom och försöker förstå varför en person huvudsakligen utvecklar minnesproblem, medan andra övervägande har t.ex. beteendeförändringar, språkstörningar eller synstörningar. För det tredje strävar vi efter att belysa mekanismerna bakom motståndskraften, det vill säga förmågan att hantera eller motstå Alzheimers sjukdomspatologi. Vi kan lära oss mycket av personer som är kapabla att upprätthålla sina kognitiva funktioner inför Alzheimers sjukdomspatologi, och kanske kan den biologiska grunden i framtiden användas för att öka motståndskraften hos mindre motståndskraftiga individer.
Vad betyder detta pris från Alzheimerfonden för din forskning?
"Det är otroligt att få denna prestigefyllda utmärkelse. Jag är mycket tacksam mot Alzheimerfonden, det är en ära att nu vara knuten till de tidigare mottagarna, som alla är framstående forskare som jag respekterar mycket. Jag ser denna utmärkelse som ett tecken på ett erkännande av det arbete som vår svenska BioFINDER studiegrupp utfört och vill tacka hela teamet för deras fantastiska bidrag. Detta pris är en stor motivation att fortsätta och till och med påskynda vår forskning."

Sebastian Palmqvist, överläkare vid Minneskliniken, Skånes universitetssjukhus och docent vid Lunds universitet
Sebastian Palmqvist, har 2023 tilldelats 1 miljon kronor från Alzheimerfonden för att fortsätta en studie kring alzheimerdiagnostisk inom primärvården.
"Det är en världsunik studie. Pengarna från fonden skapar helt nya möjligheter för forskargruppen", säger Sebastian Palmqvist.
En person som drabbas av kognitiv svikt vänder sig i första hand till sin vårdcentral. Men i primärvården har läkarna fortfarande idag 2024 trubbiga verktyg för att ställa rätt diagnos – bland annat ett minnestest som utformades i mitten av 1970-talet. Forskning har visat att det är väldigt svårt att identifiera Alzheimer med nuvarande primärvårdsverktyg, speciellt i ett tidigt skede.
"Det är absolut ingen kritik mot primärvårdsläkarna, jag är specialistläkare men hade inte gjort det bättre själv. Att skilja alzheimer-symptom från vanlig åldersrelaterad kognitiv svikt är svårt. Att nuvarande riktlinjer säger att primärvårdsläkarna ska diagnosticera den allvarliga sjukdomen med så dåliga verktyg är inte riktigt schysst", säger Sebastian Palmqvist.
För fyra år sedan inledde han studien där ett 20-tal vårdcentraler i Skåne deltar och 1 200 patienter kommer att ingå fram till år 2026.
"Vår studie är världsunik på det sättet att patienterna efter att ha träffat en läkare inom primärvården där de gör kognitiva tester och tar blodprov går vidare till en minnesklinik där det gör en fullständig undersökning med ryggvätskeprov eller PET-kamera och utredning av en specialist. Det gör att vi får en referensstandard – en standard vi kan använda för att bedöma patienternas tester och blodprov och identifiera Alzheimer korrekt."
När data från 500 patienter nu analyserats ser man att det blodprov som nu testats inom primärvården ger en mycket bättre träffsäkerhet. I det enkla provet kan man avläsa proteinet tau i blodet – hos en person med Alzheimers sjukdom är värdet ungefär sju gånger högre än hos en kontrollgrupp.
"Det ser väldigt lovande ut. Med hjälp av blodprovet identifierar vi fler än 90 procent av patienterna som har en begynnande sjukdom. I slutet av året hoppas vi att blodprovet ska vara tillgängligt i hela landet. Sahlgrenska universitetssjukhuset i Göteborg blir sannolikt först med att införa det nationellt i klinisk praxis", säger Sebastian Palmqvist.
Det svenskutvecklade läkemedlet mot Alzheimers sjukdom, lecanemab, har redan blivit godkänt i USA, Japan och Kina. Inom kort väntas även den europeiska läkemedelsmyndigheten ta beslut kring godkännande och därefter skulle läkemedlet kunna bli tillgängligt Sverige. Analys av tillgängliga data visar att lecanemab bara har tydlig effekt om det sätts in tidigt i sjukdomsförloppet.
Vad hoppas du uppnå med din forskning?
"Blir läkemedlet tillgängligt kommer allt fler att vilja testa sig. Då blir det ännu viktigare att kombinera blodprover med enkla minnestester i ett tidigt skede för att snabbt och med större säkerhet kunna remittera till specialistvården."
Sebastian Palmqvist berättar att inom ramen för studien kommer även nya kognitiva tester utvecklas – alltifrån enkla tester med papper och penna till avancerade tester för telefoner och surfplattor. Ännu en målsättning är att utarbeta prognostiska verktyg.
"Med hjälp av algoritmer hoppas vi kunna bedöma hur hög risk en patient löper att drabbas av sjukdomen de närmaste åren och hur sjukdomen kommer
att utvecklas. Vi kommer att följa våra patienter över fyra års tid", avslutar Sebastian Palmqvist.
2019 var Sebastian Palmqvist årets pristagare av "Drottning Silvias pris till en ung alzheimerforskare". Priset på motsvarande 125 000 kronor fick han till sin betydande forskning kring förbättrad diagnostik inom primärvården.

Joana Pereira, Biträdande Lektor, Karolinska Institutet
Det är viktigt att identifiera Alzheimers sjukdom så tidigt som möjligt för att stoppa dess progression innan det är för sent. Fokuset för Joanas forskargrupp är att identifiera de tidigaste förändringarna i hjärnans synapser (nervcellskopplingspunkter) hos individer som riskerar att utveckla AD och fastställa huruvida förändringarna kan användas för att förutsäga utvecklingen till AD. Det görs genom att rekonstruera nätverket av nervcellsanslutningar hos individer som visar tecken på aggregering av giftiga proteiner associerade med AD, men som ännu inte har några kliniska symptom.
Genom att bygga kopplingsschemat med data från magnetisk resonansavbildning (MR) och bestämma hur den giftiga proteinansamlingen skadar hjärnans kopplingar, kan de använda den informationen för att skapa en MR-sjukdomsindikator som kan förutsäga uppkomsten av AD i olika grupper av kognitivt friska individer. Eftersom MR är en icke-invasiv metod som enkelt kan användas utan att utgöra en alltför stor belastning för patienterna, kommer MR sjukdomsindikator att ge en stor klinisk fördel. De kommer även att göra denna sjukdomsindikator offentligt tillgänglig så att andra kliniker och forskare kan använda den för att diagnostisera AD i tidiga skeden.

Gemma Salvadó, postdoktor vid Institutionen för kliniska vetenskaper Lunds universitet
Snabbare och säkrare diagnoser är ett första mål för Gemma Salvadós forskningsprojekt som sker i samarbete med Washington University. Den spanska forskaren, verksam vid Lunds universitet, fick 2022 ett anslag på en miljon kronor från Alzheimerfonden.
"Det var en rolig överraskning. Jag fick min forskningstjänst i Sverige som postdoktor för bara ett år sedan så jag känner mig både tacksam och hedrad av anslaget. Jag tror att mitt forskningsprojekt kan få betydelse både i det korta och långa perspektivet", säger Gemma Salvadó som kommer från Barcelona och som sedan ett år tillbaka forskar vid Lunds universitets avdelning för klinisk minnesforskning.
Verktygen för att diagnosticera en patient med Alzheimers sjukdom och förutspå hur sjukdomen kommer att utvecklas är fortfarande trubbiga. De undersökningar som görs på Minneskliniker är ofta både kostsamma och invasiva och möjligheten för patienten att få en tillförlitlig diagnos är mycket varierande beroende på var i landet du bor.
Med sitt forskningsprojekt vill Gemma Salvadó förbättra möjligheterna till snabbare och säkrare diagnoser som hon hoppas ska bli mer tillgängliga för hela befolkningen. Utgångspunkten är den svenska Biofinderstudien* vars främsta syfte är att utveckla metoder för tidig diagnostik och i förlängningen botemedel mot neurodegenerativa sjukdomar som Alzheimers sjukdom. I Biofinder 1 och Biofinder 2 har nivåerna av proteinerna amyloid-beta och tau, båda viktiga markörer för utvecklingen av Alzheimers sjukdom, undersökts genom blod- och ryggvätskeprov samt med undersökningar i magnet- och PET-kamera hos cirka 1 200 deltagare.
"Vi vill jämföra resultaten från Biofinderstudierna med nya prover och se vilka biomarkörer som är lika bra på att identifiera tau-patologi i ett blodprov som i ryggvätska, men också vilka biomarkörer som kan förutsäga om sjukdomsförloppet blir långsamt eller snabbt", säger Gemma Salvadó.
En viktig samarbetspartner i projektet är Washington University School of Medicine där man är världsbäst på att identifiera tidiga tecken på Alzheimers sjukdom genom att analysera blodprover men även på att jämföra biomarkörer i blodet med biomarkörer från ryggvätskeprov och PET-kameraundersökningar. Proverna från de svenska deltagarna kommer att sändas till Washington för analys.
"Styrkan i forskningsprojektet är att vi har många patienter och data som sträcker sig åtta år tillbaka i tiden men också att vi studerar och jämför många olika biomarkörer i många olika sorters prover", säger Gemma Salvadó
Vad hoppas du uppnå med forskningsprojektet?
"Våra resultat ser lovande ut. I det korta perspektivet hoppas jag att patienter ska kunna få snabbare diagnoser utan att behöva ta ryggvätskeprov eller göra undersökningar i PET-kamera och att blodprover så småningom kommer att användas rutinmässigt i primärvården för diagnoser"
"I det långa perspektivet hoppas jag att projektet kan hjälpa till att rekrytera deltagare till nya studier med antikroppsbehandlingar som kan hejda sjukdomen eller göra att den bryter ut senare."
* Biofinderstudien är ett samarbete mellan bland annat Minneskliniken på Skånes universitetssjukhus och Sahlgrenska akademin vid Göteborgs universitet.

Michael Schöll, professor vid Göteborgs universitet
I april 2024 gick startskottet för projektet REAL AD i Västra Götalandsregionen där Alzheimerfonden är en av bidragsgivarna. Målet med den stora studien är att undersöka om det går att införa bättre diagnosverktyg inom primärvården men även om screening för tidig Alzheimers sjukdom är möjlig när nya behandlingar finns att tillgå.
"50-80 procent av alla Alzheimerdiagnoser ges inom primärvården av läkare som har undersökt patienten i tio minuter. Vi befinner oss i ett läge där vi har bra biomarkörer och lovande digitala kognitiva tester, men de används inte på vårdcentraler. Vi måste få in forskningsframstegen i vården när dessa är validerade och därmed demokratisera tillgången till de verktyg som finns", säger Michael Schöll, professor vid sektionen för psykiatri och neurokemi Göteborgs universitet.
Det är Michael Schöll som har designat studien REAL AD som nyligen firade ett år och kommer att pågå ytterligare tre. Det är ett enormt arbete som ligger bakom projektet som har en budget på över 100 miljoner kronor. Målsättningen var från början att få med sig ett brett befolkningsunderlag och ett stort antal primärvårdsenheter, berättar Michael Schöll. Han gick direkt på de högsta beslutsfattarna inom Västra Götalandsregionen och lyckades efter enträget påverkansarbete få med sig hela Närhälsan, den primärvård regionen äger och driver i egen regi, med fler än hundra vårdcentraler i Västsverige.
"Det är ett ofantligt komplext projekt. Vi har till exempel utbildat över 1 200 personer inom vården hur de ska hantera blodprover, vi har skapat en innovativ plattform för deltagarna och till och med skapat eget faktureringssystem för att kunna betala för varje blodprov som tas i studien."
"Många tyckte i början att det var fullständig idioti med en sådan stor och komplicerad studie, men när jag tror på något har jag svårt att sluta. Den diagnostik som sker inom primärvården idag är inte så bra som den kan vara, den spetsforskning som finns i Sverige har hittills ofta förblivit teori och kommer inte ut i kliniken vilket gör att patienterna inte får den vård de skulle kunna få."
Målsättningen med REAL AD är att undersöka möjligheten att implementera de nya diagnostiska verktygen inom primärvården. Det gäller både de digitala minnestester som finns idag och diagnostisk med biomarkörer som kan göras med ett enkelt blodprov. Ännu ett syfte med studien är att undersöka om de tillgängliga diagnostiska verktygen gör det möjligt att i framtiden screena personer i medelåldern för att hitta de som kan ha mest nytta av de läkemedel som förmodligen kommer att finnas i framtiden.
"Är det rimligt att screena? Ska vi ens tänka oss det? Det beror på hur behandlingslandskapet kommer att se ut och hur bra våra verktyg faktiskt är. Jag anser ändå att vi måste förbereda oss för den möjligheten – som det ser ut idag är vi inte särskilt förberedda2, säger Michael Schöll.
När REAL AD presenterades i april 2024 fick projektet stort genomslag i medierna och intresset från allmänheten var lika stort. Över 7 000 personer i åldersgruppen 50–80 år anmälde initialt sitt intresse för att delta genom att göra kognitiva tester hemma med hjälp av en mobilapplikation och i nästa steg besöka sin vårdcentral för att lämna blodprov. De blodprov som lämnas analyseras med de biomarkörer som kan identifiera om person har eller riskerar att få Alzheimers sjukdom.
"Just nu har vi cirka 3 500 deltagare som vill genomföra hela studien som pågår i ytterligare cirka tre år. Ur den gruppen kommer vi även rekrytera cirka 400 personer som går vidare till ett valideringssteg. De deltagarna kommer att göra undersökningar i PET- och magnetkamera, lämna ryggvätskeprov och träffa vårdpersonal vid två tillfällen under fyra år."
Ser du screening för Alzheimers sjukdom som en framtida möjlighet?
"Studien är en av flera som undersöker möjligheten, det finns många aspekter som måste lösas innan det kan bli realitet men om det finns en relativt billig, säker och skalbar behandling kan incitamentet finnas. Metoderna vi undersöker i REAL AD är inte dyra och är direkt skalbara."
När kan REAL AD blir en verklighet i hela Sverige?
"Vi har försökt att designa studien så att upplägget skulle kunna köra i gång så lätt och så snabbt som möjligt. Det är dock inte jag som fattar sådana beslut, men när beslutsfattarna väl säger ja till detta har vi en unik möjlighet att utveckla den här metoden eller i alla fall en liknande inom primärvården."
Vad betyder Alzheimerfondens anslag på 1,3 miljoner kronor för projektet?
"Det är jätteviktiga pengar. De behövs bland annat till dyra analyser och löner. Det är en extremt dyr studie eftersom vi har börjat från scratch."
FAKTA
REAL AD drivs av Michael Schöll, Kaj Blennow, Henrik Zetterberg och Silke Kern tillsammans med ett team av projektledare och forskare, VGR Närhälsan och ett antal samarbetspartner inom akademin och läkemedelsindustrin.

Dag Sehlin
Dag Sehlin, professor vid Uppsala universitet
Dag Sehlin, professor vid Institutionen för folkhälso- och vårdvetenskap Uppsala universitet, har tilldelats 1,3 miljoner kronor för att utveckla bispecifika antikroppar för behandling och diagnos av Alzheimers sjukdom.
"Det är särskilt roligt att få stöd från Alzheimerfonden som har Sveriges främsta Alzheimerexperter i sitt vetenskapliga råd. Att få ett anslag av dem är den största uppmuntran man kan få och inger känslan att man är på rätt väg", säger Dag Sehlin.
Dag Sehlin är en av de viktigaste forskarna bakom det första sjukdomsmodifierande läkemedlet för Alzheimers sjukdom – antikroppen Lecanemab – som han har arbetat med under tjugo års tid. Nästa steg i utvecklingsarbetet har varit att ta fram en modifierad antikropp som han beskriver som en trojansk häst syftande på att den kan åka snålskjuts med kroppens eget transportsystem in i hjärnan. Den nya antikroppen bi-lecanemab som är en modifiering av lecanemab hakar på den så kallade transferrinreceptorn (TfR) och kan därigenom ta sig in bakom blod-hjärnbarriären i mycket större mänger.
Bilder från forskargruppens studier i musmodeller visar en tydlig skillnad mellan de båda antikropparna.
"Jämfört med lecanemab distribueras bi-lecanemab jämnt till hela hjärnan genom dess vidsträckta kärlträd och i mycket större mängder", säger Dag Sehlin och fortsätter:
"Mus och människa är inte samma sak och vi måste komplettera med andra studier bland annat i mänskliga cellmodeller. Men vi tror extra mycket på vår musmodell – att det liknar det som skulle uppträda i en mänsklig hjärna med Alzheimers sjukdom."
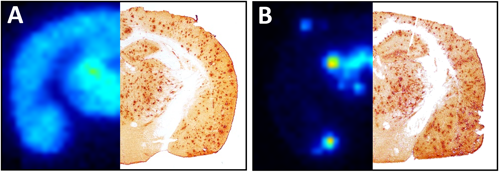
Bildtext:
A. Den modifierade, bispecifika antikroppen distribueras jämnt i hela hjärnans volym (vänster bildhalva) där den binder till plack (höger bildhalva). B. Den vanliga antikroppen uppvisar en ojämn distribution och återfinns framförallt i hjärnans inre delar samt kring stora blodkärl i hjärnan.
Som utvecklat läkemedel skulle vinsterna vara stora – preparatet skulle kunna vara mer effektivt, kunna ges i lägre doser och även ge mindre biverkningar.
"Men vi vet inte hur den kognitiva förmågan påverkas. Tar den bispecifika antikroppen bort placken på bekostnad av hjärncellernas hälsa? Vår hypotes är att antikroppen verkar med hjälp av gliaceller, vilket skulle kunna påverka inflammationen i hjärnan – den vill vi inte förvärra. Hur ser mekanismerna ut och vad kan vi göra för att förhindra eventuella skadliga processer?"
Syftet med projektet som Alzheimerfonden beviljat ett stort anslag till är just att kartlägga hur antikropparna interagerar med amyloid-beta och olika celltyper i hjärnan. Men även att studera stödjecellerna mikroglias roll i nedbrytningen av de amylodia placken. I projektet ingår också att designa en PET-radioligand baserad på bi-lecanemab som kan användas vid framtida diagnostik.
Bilecanemab låter som ett viktigt steg framåt för att kunna bromsa sjukdomen!
"Det känns rimligt att den kan fungera ännu bättre att ta bort placken, att vi genom tidiga och precisa diagnoser skulle kunna förhindra och fördröja sjukdomen ännu mer. Men många processer i hjärnan fortsätter även om man tar bort placken. Så antikroppen kan behöva kombineras med andra läkemedel mot till exempel tau-patologi, neuroinflammation och synapsdegeneration."

Ingmar Skoog, seniorprofessor vid Göteborgs universitet
Ingmar Skoog, seniorprofessor inom psykiatri vid Göteborgs universitet, är en av de forskare Alzheimerfonden beviljat anslag till under ett flertal år. 2024 tilldelades han en halv miljon kronor för att fortsätta en studie där han följer personer födda 1944. Syftet är att öka kunskapen om de biologiska processerna innan symtom på Alzheimers sjukdom bryter ut.
Idag är Ingmar Skoog kanske mest känd som ständig bisittare i SVT:s Studio 65 och författare till den hoppingivande boken ”70 är det nya 50”. Men 71 år fyllda har professorn och föreståndaren för Age Cap trots ett hektiskt schema med tv-inspelningar och utlandsresor inga planer på att lämna forskarvärlden.
Det var något av en slump att han som 30-årig läkare ramlade in i den stora befolkningsstudien H70. Studien var först i världen att hitta samband mellan Alzheimers sjukdom och högt blodtryck, övervikt och stress. Då fick han träffa och intervjua personer födda i början av det förra seklet. Idag är det 40-talister, födda 1944, han sysselsätter sig med.
Den studie han nu har fått anslag för drogs i gång 2014 med syftet att öka kunskaperna om så kallad preklinisk Alzheimers sjukdom. Genom att följa deltagare från 70 års ålder och flera decennier framåt hoppas Ingmar Skoog och hans team få ledtrådar till varför sjukdomen bryter ut hos vissa men inte hos andra.
Deltagarna som följs upp med fem års intervaller har studerats ingående. Hur är det med hörsel, syn, kosthållning, psykiskt och fysiskt välbefinnande, genetik, sömnvanor, språk och kognition? De har även undersökts med PET- och magnetkamera och fått lämna blod- och ryggvätskeprov.
"Vi har åtta sjuksköterskor som arbetar med studien. Idag har vi flera deltagare på plats - de brukar stanna i åtta timmar", berättar Ingmar Skoog, när vi ses på hans arbetsplats, Centrum för åldrande och hälsa, Age Cap, i Mölndal utanför Göteborg.
Genom studien har Ingmar och hans team en unik möjlighet att studera vad som händer innan en person utvecklar Alzheimers sjukdom:
"Det är så många olika parametrar som spelar in. Vi hoppas kunna se mönster. Vad är det som händer i kroppen och varför får vissa sjukdomen, andra inte? Vi hoppas att studien ska ge oss ledtrådar till hur vi kan förebygga sjukdomen och ta fram nya behandlingar."
Nivåerna av beta-amyloid och p-tau i blod- och ryggvätskeprov, biomarkörer för att upptäcka patienter med Alzheimers sjukdom, är en av parametrarna som studeras. Men även volymen på hippocampus (det område i hjärnan som är viktigt för minne och inlärning), muskelmassa, blodtryck, psykiskt mående, gånghastighet och BMI undersöks för att upptäcka samband med när kognitiva svårigheter uppkommer och en person insjuknar.
De preliminära resultaten från femårsuppföljningen är glädjande. Bland studiens cirka 900 deltagare hade 48 personer sjukliga nivåer av beta-amyloid. Men det var endast 3 personer av dem, eller sex procent, som insjuknade i demens.
"Många av dem som har patologiska nivåer av beta-amyloid utvecklar inte en demenssjukdom. Det är färre som har insjuknat än vi trodde, när vi nu analyserar 80-åringarna kommer det antagligen vara fler. Risken är alltså extremt liten på kort sikt."
"Vår tolkning är att sjukliga nivåer av beta-amyloid inte räcker för att utveckla sjukdomen. Har man även riskgenen APOE4 och sömnstörningar ökar risken betydligt. Vi ser också ett samband med volymen på hippocampus. Om den minskar, och personen har förhöjda nivåer av beta-amyloid, samt nivåerna av p-tau sticker i väg då börjar man se förändringar i kognitionen", säger Ingmar.
I mer än fyra decennier har han forskat kring äldre och åldrande och sett hur samhällsförändringar påverkat våra möjligheter att vara friska och må bra långt upp i åldern. En högre utbildningsnivå, bättre behandlingar av högt blodtryck och stroke är faktorer som bidragit till att dagens 85-åringar är mycket friskare än de var på 1980-talet. Risken för att drabbas av en demenssjukdom efter 85 har minskat med 40 % sedan 1986.
Trots det ser framtiden mörk ut. Vi står inför en explosiv befolkningsutveckling i gruppen 80+. Under en femårsperiod beräknas antalet personer som är 80 år och äldre att öka från cirka 600 000 till omkring 800 000.
"Så även om andelen som insjuknar minskar så kommer vi att få fler och fler äldre som har en demenssjukdom vilket för med sig enorma samhällskostnader och ett stort behov av att prioriteringar inom sjukvården."
Engagemanget för de äldre och glädjen i forskningen verkar inte mattas av hos Ingmar Skoog. Pensioneringen ser ut att få vänta ett tag till:
"Det är fortfarande lika spännande och kul att se vad man hittar. Jag vill gärna följa mina 70-åringar fram tills att de fyller 85 om fyra år - det skulle kännas som att sluta cirkeln."
Ruben Smith
Ruben Smith, docent vid Lunds universitet
Ruben Smith, docent i neurologi vid Lunds universitet, har fått ett anslag på 1,1 miljoner kronor från Alzheimerfonden. Pengarna ska gå till att utveckla och utvärdera nya biomarkörer för neurodegenerativa sjukdomar som ofta samexisterar med Alzheimers sjukdom.
De senaste åren har metoderna för att diagnosticera Alzheimers sjukdom tagit ett stort kliv framåt. Idag kan man med hjälp av PET-kamera, prov på ryggmärgsvätska eller ett enkelt blodprov konstatera om en patient har de för Alzheimers sjukdom karakteristiska placken av amyloid-beta och så kallade taupatologier. Idag finns också terapier som kan användas för att bromsa sjukdomsutvecklingen.
Under senare år har dock forskarna konstaterat att många patienter som har Alzheimers sjukdom även har andra sjukliga förändringar i hjärnan. Det kan till exempel röra sig om ansamlingar av proteinet α-synuklein som bildar aggregat och kan ge upphov till både Lewykroppsdemens och Parkinsons sjukdom. Det kan också handla om vaskulära förändringar. Hos patienter med flera patologier ser den kognitiva försämringen även ut att ske snabbare.
–Har man en ”ren” Alzheimer svarar man bättre på en behandling. När fler behandlingar kommer ut på marknaden blir det allt viktigare att kunna verifiera vilka patologier som en patient har. Ju mer vi vet desto mer specifika kan vi vara när vi sätter in behandlingar, säger Ruben Smith och fortsätter:
– Man kan säga att vårt projekt syftar till att komma närmare det vi kallar Personalized Medicine eller skräddarsydd precisionsmedicin.
I projektet kommer Ruben Smith och hans forskargrupp arbeta brett för att utveckla och identifiera nya biomarkörer. I dagsläget finns till exempel inget enkelt sätt att diagnosticera den relativt nyligen upptäckta neurodegenerativa sjukdomen LATE som är en förkortning av Limbic-predominant age-related TDP-43 encephalopathy. Sjukdomen drabbar ofta äldre patienter och påverkar till skillnad från Alzheimers sjukdom nästan bara minnet.
– Vid obduktioner har vi sett att ansamlingar av proteinet TDP-43 är mycket vanligt, men ännu har vi inga riktigt bra markörer för att identifiera det under livet. I det här projektet kommer vi att samarbeta med ett schweiziskt företag som utvecklat en PET-radioligand, en radioaktiv markör, som kan påvisa olika typer av TDP-43 vid PET-undersökningar.
–Det vore ett stort lyft om vi kunde diagnosticera patienter genom PET-undersökningar men också i framtiden genom blodprov och i förlängningen om det också kunde komma en behandling mot TDP-43.
För att närma sig målet att identifiera nya biomarkörer för sjukdomar som vanligtvis samexisterar med Alzheimers sjukdom kommer Ruben Smiths forskargrupp studera stora individgrupper. I en delstudie ingår personer med och utan Alzheimers sjukdom som har konstaterat förhöjda nivåer av det skadliga proteinet α-synuklein.
I en annan delstudie kommer en grupp patienter från BioFinder sömnstudien, som startade 2021, att ingå. Dessa patienter med milda sömnstörningar har en ökad risk att utveckla Parkinsons sjukdom.
Båda grupperna kommer att genomgå kognitiva tester, undersökas genom blod- och ryggvätskeprovtagning och avbildning med magnetkamera och PET. Deltagarna kommer att följas upp under sex års tid.
– Stora studier gör det möjligt att titta på flera faktorer samtidigt och generar större datamängder som gör det lättare att se sambanden. Eftersom vi följer dessa personer över tid hoppas vi också identifiera markörer för olika stadier i sjukdomsutvecklingen.
Vad betyder anslaget från Alzheimerfonden?
–Det är väldigt glädjande och mycket viktigt för att vi ska kunna göra så här stora, kostsamma studier. Anslaget hjälper till att höja hastigheten för att komma närmare målet att kunna identifiera sjukdomar på ett individuellt plan, hitta nya biomarkörer och kunna sätta in behandlingar där de har bäst effekt.

Alina Solomon, docent i neuroepidemiologi, Karolinska Institutet
Alina Solomon, docent i neuroepidemiologi, verksam vid Karolinska Institutet och Östra Finlands universitet har 2020 beviljats 1,9 miljoner kronor i forskningsbidrag från Alzheimerfonden.
"Jag är otroligt glad över pengarna från Alzheimerfonden. Tack vare dem kan förutom Finland och Storbritannien även Sverige och Karolinska Institutet medverka i vår nya interventionsstudie", säger Alina Solomon.
I september hoppas hon kunna sätta igång den nya tvååriga studien som är en fortsättning på den mycket uppmärksammade FINGER-studien. FINGER var den första interventionsstudien i världen som visade att kostråd, fysisk och kognitiv träning samt kontroll av vaskulära riskfaktorer som högt blodtryck, blodsocker och blodfetter kan förebygga kognitiv försämring i hjärnan. I den nya studien vill Alina Solomon och hennes forskargrupp undersöka om en kombination av livsstilsåtgärder och läkemedel kan förebygga kognitiv svikt.
Sex hundra personer i åldrarna 60-77 som har riskfaktorer för demens men ännu inte har någon uttalad kognitiv svikt kommer att delta. En andel av deltagarna kommer förutom att arbeta med livsstilsfaktorer få en daglig dos av läkemedlet metformin. Läkemedlet används idag för behandling av diabetes, som anses vara en av flera riskfaktorer för att utveckla Alzheimers sjukdom.
Innan studien påbörjas och efter att den är slutförd kommer deltagarna i metformingruppen att genomgå en undersökning med PET- eller magnetkamera. Med hjälp av biomarkörer hoppas forskarna kunna se vilken effekt läkemedlet i kombination med livsstilsåtgärder kan ha.
"Ger läkemedlet bättre effekt och i så fall hur mycket bättre? Vi hoppas få svar som hjälper oss att skapa behandlingar som kombinerar livsstil med läkemedel. Vi tror inte att det finns någon magic bullet, något enskilt läkemedel som kan bota Alzheimers sjukdom. Vi tror att vi i framtiden behöver kombinera åtgärder anpassade till varje persons riskprofil. Det här är ett steg vidare på vägen."

Stina Syvänen, professor vid Uppsala universitet
Stina Syvänen, professor inom molekylär geriatrik, har beviljats ett anslag på 850 000 kronor för att utveckla biospecifika antikropp-PET-radioligander. Målet är förbättrad diagnostik och behandling av neuroinflammatoriska processer vid Alzheimers sjukdom.
Den medicinska avbildningstekniken positronemissionstomografi (PET) har varit ett viktigt verktyg för utvecklingen av nya läkemedelskandidater mot Alzheimers sjukdom. Vid PET-scanning används radioaktivt märkta molekyler så kallade radioligander som binder till proteinstrukturer som är typiska för ”kärnan” i den amyloida placken. Med PET-diagnostik kan man alltså se om en patient har de typiska placken vid Alzheimers sjukdom men också studera effekten efter en behandling med till exempel bromsmedicinen Lecanemab.
Det är forskargruppen i Uppsala som har utvecklat antikroppen mAb158 som är ”förlagan” till Lecanemab. De har också utvecklat en ny generation antikroppar så kallade bispecifika antikroppar som genom att binda till transferrinreceptorn tar sig över blod-hjärnbarriären i större mängder. Jämfört med en monoklonal antikropp ökar antikroppskoncentrationen i hjärnan med upp till åttio gånger vilket är en stor framgång för både terapi och diagnostik.
– Det här är superviktigt för läkemedelsutvecklingen. Just nu pågår en tysk studie där bispecifika antikroppar används som PET-radioligander för att diagnosticera cancertumörer i hjärnan. Det ska bli intressant att se hur de lyckas. Frågeställningarna är ju likadana inom alzheimerforskningen, säger Stina Syvänen.
Stina och hennes team var först i världen med att visa att man kan använda bispecifika antikroppar som PET-radioligander för att avbilda giftiga lösliga former av amyloid-beta, så kallade protofibriller. Idag tror forskarna att de här amyloida aggregaten som är mindre än plack och fortfarande lösliga kan vara mer skadliga för hjärnan än placken. En hypotes är att aggregering av amyloid-beta aktiverar hjärnans immunceller vilket kan leda till utspridd och kronisk neuroinflammation.
I det nya projektet, som fått anslag från Alzheimerfonden, är målet att utveckla PET-radioligander som kan detektera andra sjukdomsrelaterade protein i hjärnan kopplade till just neuroinflammation.
– Hjärnans stödjeceller astrocyter och mikroglia kämpar hårt mot inflammationen. Vi behöver nya PET-radioligander för att förstå sjukdomsprocesserna bakom inflammationen. Det är här jag tror behovet av nya läkemedel finns. Jag tror att framtidens behandling av Alzheimers sjukdom kommer att vara en kombination av läkemedel riktade mot amyloid-beta som Lecanemab och läkemedel som dämpar inflammation – kanske tillsammans med läkemedel mot tau och preparat som boostar synapserna och nervellerna.

Jacob Vogel
Jacob Vogel, Assistant professor, Lunds universitet
Jacob är från Philadelphia men tog sin doktorsexamen i Kanada. Under sin praktik på ”Alzheimer center” i Amsterdam fick han möjlighet att besöka Sverige, här träffade han professor Oskar Hansson och hans team. Idag är Jacob själv en del av teamet på Lunds universitet.
Den 15 november 2023 tilldelades Jacob ”Drottning Silvias pris till en ung alzheimerforskare”, en fin utmärkelse med en prissumma på 500 000 kronor. Jacob berättar att pengarna ska gå till att effektivisera forskningen i labbet. Jacob har startat ett labb vid Lunds universitet, som en del av SciLifeLab och Wallenberg National Program for Data-driven Life Science.
Hur känns det att vinna "H.M. Drottning Silvias pris till en ung alzheimerforskare"?
"Jag känner mig väldigt tacksam. Att få ta emot detta pris som ung betyder mycket för motivationen och jag känner mig inspirerad. Jag vill göra er på Alzheimerfonden stolta och fortsätta med min forskning. Att få detta ärofyllda pris och få träffa H.M. Drottningen blir som en drivkraft och jag känner att jag är på rätt spår i min karriär. Det är också väldigt roligt att få besöka Alzheimerfondens kontor och se hur ni arbetar.”
Trots att Jacob Vogel fortfarande är i ett tidigt skede av sin karriär har han redan hunnit bidra med flera viktiga upptäckter till alzheimerforskningen. Bland annat har han lett en mycket inflytelserik studie som visade att förändringar i hjärnan relaterade till Alzheimer varierar från person till person. Denna har nu lett forskarna att tro att det finns fyra olika ”typer” av Alzheimers sjukdom, en insikt forskarna hoppas ska kunna hjälpa till i utformningen av mer patientanpassade behandlingar. Upptäckten har gett upphov till många nya typer av undersökningar världen över och det huvudsakliga arbetet i Jacobs labb är just att försöka förstå de biologiska mekanismer som ligger till grund för de olika sjukdomstyperna så att forskarna kan utveckla lämpliga behandlingsmetoder.
”Mitt arbete handlar väldigt mycket om att analysera data som samlats in från patienter. Det arbete jag försöker göra är att samla ihop olika former av biologisk data, bilder av hjärnan, proteininformation från blod och även genetik. Med dessa olika delar kan vi få en mer nyanserad bild och förstå och få fram den här komplicerade bilden av vad som händer i hjärnan. I mitt labb försöker vi verkligen skapa modeller som kommer att förutsäga förloppet eller utvecklingen av Alzheimers sjukdom och använda informationen till att svara på frågor som exempelvis, hur börjar sjukdomen, vilken del av hjärnan startar den i? Vem kommer att få sjukdomen och när, och så vidare.”
Jacob Vogel är även en av de främsta experterna inom tau-avbildning. Tau-proteinet verkar vid Alzheimers sjukdom vara inblandat i att skada hjärnceller och leda till kognitiva nedsättningar. Forskarna kan nu avbilda tau-proteinet i hjärnan hos levande människor med en teknologi som kallas PET. Jacob var inblandad i några av de tidigaste studierna som karaktäriserade tau-PET i den mänskliga hjärnan och är fortfarande en auktoritet inom ämnet. Särskilt anmärkningsvärt är att Jacob lånade tekniker från den vetenskapliga litteraturen om infektionssjukdomar och tog fram mycket övertygande evidens som visade att patologisk tau kan spridas i hjärnan genom att använda hjärnceller som ”motorvägar”. Denna teori har blivit otroligt viktig nu när forskarna är i en era av kliniska försök.
Vad är målet med din forskning?
"Jag skulle säga att ett stort huvudmål är att försöka förstå Alzheimers sjukdom på individnivå. Att skilja på individer då det kommer behöva individanpassa behandlingar. Att använda informationen om sjukdomen för att i nästa steg kunna erbjuda bättre vård."
Läs mer om Jacobs forskning och prisceremonin här.

Eric Westman, universitetslektor, Karolinska Institutet
Eric Westman, professor vid Karolinska Institutets institution Neurobiologi, vårdvetenskap och samhälle, har länge forskat kring komplexiteten och heterogeniteten i Alzheimers sjukdom.
I sin forskning kombinerar han olika hjärnavbildningstekniker med biomarkörer för att undersöka hur olika neurodegenerativa sjukdomar utvecklas över tid. Med positronemissionstomografi, så kallad PET-kamera, kan man se hur stor inlagringen av beta-amyloid och tau, båda markörer för Alzheimers sjukdom, är. Med magnetresonanstomografi (MRT), så kallad magnetkamera, kan graden av atrofi, förtvining, och förändringar i vit och grå substans visualiseras och kvantifieras, liksom hur nervcellerna och axoner kommunicerar.
"Alzheimers sjukdom är inte en homogen sjukdom utan kan delas in i olika subtyper. Under de senaste åren har forskarna allt mer uppmärksammat hur neurodegenerativa sjukdomar som Alzheimers sjukdom, Levykroppsdemens och vaskulär demens går in i och överlappar varandra. Det komplicerar möjligheterna att sätta korrekta diagnoser men också att arbeta preventivt och veta vilka läkemedel vi ska sätta in. Vi behöver bättre förståelse för heterogeniteten i sjukdomarna", säger Eric Westman.
För att upptäcka sjukdomsmönster kombinerar Eric Westman och hans forskargrupp den senaste hjärnavbildningstekniken med avancerade metoder för att avläsa bildsekvenser som till exempel kluster- och nätverksanalys och maskininlärning.
"Målet är att skapa mer avancerade metoder att ställa diagnoser som kan appliceras i den kliniska verksamheten så att patienterna kan selekteras redan där. Men också att i framtiden utveckla nya läkemedel och mer personinriktade behandlingar."
Vad betyder forskningsanslaget från Alzheimerfonden på 1,9 miljoner?
"Det är jätteviktigt. Jag har fått bidrag i några år nu. Det ger kontinuitet och stabilitet i min forskning och framför allt möjligheten att behålla anställda i min forskargrupp. Jag har tre-fyra forskare anställda i projektet."

Henrik Zetterberg, ordförande i Alzheimerfondens vetenskapliga råd
Henrik Zetterberg är ordförande för Alzheimerfondens vetenskapliga råd och den som tillsammans med övriga medlemmar i rådet föreslår vilka forskare Alzheimerfonden bör stötta.
Vilken inriktning har forskningen kring nya läkemedel idag?
Forskningen är fortfarande i mångt och mycket inriktad på att ta fram läkemedel som påverkar det protein som bygger upp de senila placken, beta-amyloid, vid Alzheimers sjukdom. Det har gått sådär, men jag anser att det är viktigt att hålla fast vid detta forskningsspår lite till och fortsätta att försöka påverka beta-amyloiden med högre doser och ännu tidigare i sjukdomsförloppet.
Kritiska forskarkollegor tycker att de negativa resultaten från långt gångna kliniska prövningar, där patienterna inte har blivit bättre av läkemedelskandidater riktade mot beta-amyloid, borde göra att man överger hypotesen om beta-amyloidens roll i sjukdomsprocessen, men jag tycker inte att hypotesen är färdigtestad ännu.
För patienternas skull är det dock viktigt att inte satsa allt på ett kort. En del forskargrupper försöker nu att angripa det protein som bygger upp neurofibriller (små trådar i nervcellerna) vid Alzheimers sjukdom. En annan möjlig behandlingsmetod skulle vara att stävja överaktiviteten hos hjärnans städarceller (mikroglia). Dessa verkar överreagera på placken vid Alzheimers sjukdom och därmed skada omkringliggande vävnad. Dessa projekt hoppas jag mycket på.
Hur der det internationella forskningsläget ut?
Det ser bra ut. Antalet forskargrupper som arbetar med Alzheimers sjukdom ökar stadigt, men vi är fortfarande förhållandevis få om man jämför med andra forskningsfält och hur många som drabbas av sjukdomen. Vi måste få in fler unga stjärnskott och stimulera forskartalanger att gå in i detta fält.
Ser du ljust på framtiden inom alzheimerforskningen?
Ja! Vi har bra biomarkörer för att studera sjukdomsprocessen över tid hos levande människor och ett stort antal möjliga behandlingar som därmed snabbt kan utvärderas hos patienter i kliniska prövningar. Jag tror att vi snart har ett eller ett par stabila genombrott i fältet, kanske redan inom ett par år. En stor fråga blir då hur dagens sjukvårdssystem skall hantera detta praktiskt och jag tror att det är viktigt att fundera på det redan nu.
